题目内容
【题目】在下列各溶液中,离子一定能大量共存的是( )
A.由水电离产生的c(H+)=1x10-13 mol/L的溶液中:Na+、K+、Cl-、SO42-
B.室温下,pH=1的盐酸中:Na+、Fe2+、NO3-、SO42-
C.含有Ca2+的溶液中:Na+、K+、CO32-、Cl-
D.常温下在KW/ c(OH-)=10-12的溶液中:K+、Al3+、Cl-、SO42-
【答案】A
【解析】
A. 由水电离产生的c(H+)=1×10-13 mol/L的溶液可以是酸性溶液,也可以是碱性溶液;
B. pH=1的盐酸存在大量的H+;
C. Ca2+与CO32-发生复分解反应;
D. c(H+)=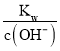 =1x10-13 mol/L的溶液为碱性溶液。
=1x10-13 mol/L的溶液为碱性溶液。
A. 由水电离产生的c(H+)=1×10-13 mol/L的溶液可以是酸性溶液,也可以是碱性溶液,酸性溶液中存在H+,碱性溶液中存在OH-,H+、OH-与Na+、K+、Cl-、SO42-均可共存,A项正确;
B. pH=1的盐酸存在大量的H+,H+、Fe2+、NO3-之间因发生氧化还原反应而不能共存,B项错误;
C. Ca2+与CO32-发生复分解反应生成白色沉淀而不能共存,C项错误;
D. c(H+)=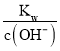 =1×10-13 mol/L的溶液为碱性溶液,存在OH-,OH-与Al3+发生复分解反应生成白色沉淀而不能共存,D项错误;
=1×10-13 mol/L的溶液为碱性溶液,存在OH-,OH-与Al3+发生复分解反应生成白色沉淀而不能共存,D项错误;
答案选A。

 一线名师提优试卷系列答案
一线名师提优试卷系列答案【题目】某同学向SO2和Cl2的混合气体中加入品红溶液,振荡,溶液褪色,将此无色溶液分成三份,依次进行实验,实验操作和实验现象记录如下:
序号 | |||
实验操作 |
|
|
|
实验现象 | 溶液不变红,试纸不变蓝 | 溶液不变红,试纸褪色 | 生成白色沉淀 |
下列实验分析中,不正确的是
A. ①说明Cl2被完全消耗
B. ②中试纸褪色的原因是:SO2 + I2 + 2H2O == H2SO4 + 2HI
C. ③中若将BaCl2溶液换成Ba(NO3)2溶液,也能说明SO2被Cl2氧化为SO42
D. 实验条件下,品红溶液和SO2均被氧化