题目内容
【题目】如图所示原电池,盐桥中装有含琼胶的KCl饱和溶液,相关的叙述中,不正确的是( )
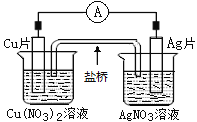
A.电子沿导线由Cu片流向Ag片
B.盐桥中的K+向Cu(NO3)2溶液
C.正极的电极反应是Ag++e-=Ag
D.Cu片上发生氧化反应,Ag片上发生还原反应
【答案】B
【解析】
A. 电子由负极流向正极;
B. 盐桥中K+向正极移动;
C. 原电池装置中Ag为正极,电解质溶液中的Ag+得到电子生成Ag;
D. 原电池装置中Cu为负极,发生氧化反应,Ag为正极,发生还原反应。
A. 原电池装置中Cu为负极,Ag为正极,电子由负极流向正极,即有Cu片流向Ag片,A项正确,不符合题意;
B. 盐桥中K+向正极移动,即K+向Ag极移动,B项错误,符合题意;
C. 原电池装置中Ag为正极,电解质溶液中的Ag+得到电子生成Ag,电极反应为:Ag++e-=Ag,C项正确,不符合题意;
D. 原电池装置中Cu为负极,发生氧化反应,Ag为正极,发生还原反应,D项正确,不符合题意;
答案选B。

 教材全解字词句篇系列答案
教材全解字词句篇系列答案【题目】下列生产或实验事实引出的相应结论不正确的是( )
选项 | 事实 | 结论 |
A | 其他条件相同,Na2S2O3溶液和H2SO4溶液反应,升高溶液的温度,析出硫沉淀所需时间变短 | 当其他条件不变时,升高反应温度,化学反应速率加快 |
B | 工业制硫酸中,在SO3的吸收阶段,吸收塔里要装填瓷环 | 增大气液接触面积,使SO3的吸收速率增大 |
C | 在容积可变的密闭容器中发生反应:2NH3(g) | 正反应速率加快,逆反应速率减慢 |
D | A、B两支试管中分别加入等体积5%的H2O2,在B试管中加入2~3滴FeCl3溶液,B试管中产生气泡快 | 当其他条件不变时,催化剂可以改变化学反应速率 |
A. A B. B C. C D. D