题目内容
有A、B、C、D四种元素,A元素的气态氢化物分子式为RH4,其中R的质量分数为75%,该元素核内有6个中子,能与B形成AB2型化合物,B在它的氢化物中含量为88. 9%,核内质子数和中子数相等,C、D为同周期元素,D的最高价氧化物的水化物为酸性最强的酸,C的氧化物为两性氧化物。
(1)A元素的一种无色透明的单质,名称叫_____,其晶体类型是________。B的氢化物的电子式为 _____________,属________(填“极性”或“非极性”)分子。
(2)A和B形成化合物的分子空间构型为_______,属________分子(填“极性”或“非极性”),其晶体类型是___________。
(3)C元素位于周期表中第____周期_____族,A、C、D三元素的最高价氧化物的水化物按酸性由强到弱的顺序排列(用分子式表示)_____________。
(4)C和D的化合物溶于水后滴入过量KOH,现象是__________,离子方程式_______________________。
(1)A元素的一种无色透明的单质,名称叫_____,其晶体类型是________。B的氢化物的电子式为 _____________,属________(填“极性”或“非极性”)分子。
(2)A和B形成化合物的分子空间构型为_______,属________分子(填“极性”或“非极性”),其晶体类型是___________。
(3)C元素位于周期表中第____周期_____族,A、C、D三元素的最高价氧化物的水化物按酸性由强到弱的顺序排列(用分子式表示)_____________。
(4)C和D的化合物溶于水后滴入过量KOH,现象是__________,离子方程式_______________________。
(1)金刚石;原子晶体;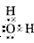 ;极性
;极性
(2)直线形分子;非极性;分子晶体
(3)3;ⅢA;HClO4>H2CO3>Al(OH)3
(4)先有白色沉淀,滴入过量KOH时白色沉淀消失; Al3++3OH-=Al(OH)3↓ Al(OH)3+OH-= AlO2-+2H2O
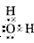 ;极性
;极性(2)直线形分子;非极性;分子晶体
(3)3;ⅢA;HClO4>H2CO3>Al(OH)3
(4)先有白色沉淀,滴入过量KOH时白色沉淀消失; Al3++3OH-=Al(OH)3↓ Al(OH)3+OH-= AlO2-+2H2O

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目




