题目内容
【题目】现有一块已知质量的铝镁合金,欲测定其中镁的质量分数,几位同学设计了以下三种不同的实验方案:
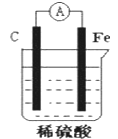
实验方案①:铝镁合金![]() 测定生成的气体在标准状况下的体积
测定生成的气体在标准状况下的体积
实验方案②:铝镁合金![]() 测定生成的气体在标准状况下的体积
测定生成的气体在标准状况下的体积
实验方案③:铝镁合金![]() 溶液
溶液![]() 过滤、洗涤、干燥后测定得到沉淀的质量
过滤、洗涤、干燥后测定得到沉淀的质量
对能否测定出镁的质量分数的实验方案判断正确的是( )
A. 都能B. 都不能C. ①不能,其它都能D. ②③不能,①能
【答案】A
【解析】
已知质量的铝镁合金,设计1、2中,利用金属的质量、氢气的量可计算出镁的质量,以此得到质量分数;设计3中,沉淀的质量为氢氧化镁,元素守恒可知镁的质量,以此得到质量分数,即三个实验方案中均可测定Mg的质量分数,A项正确,
答案选A。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】下表是不同温度下水的离子积常数,试回答以下问题:
温度(℃) | 25 | t1 | t2 |
水的离子积常数 | 1×10-14 | α | 1×10-12 |
(1)若25<t1<t2,则α______(填“<”“>”或“=”)1×10-14。
(2)25℃下,某Na2SO4溶液中c(SO42-)=5×10-4mol·L-1,取该溶液1mL,加水稀释至10mL,则稀释后溶液中c(Na+):c(OH-)=________。
(3)25℃下,将pH=1的盐酸溶液和pH=5的盐酸溶液等体积混合,则混合液中水电离出的c(OH-)=________。
(4)将t2℃温度下pH=11的苛性钠溶液a L与pH=1的稀硫酸溶液bL混合,所得混合溶液pH=2,则a:b=______;此溶液中离子浓度的由大到小的排列顺序是______________________________。(以上均忽略溶液混合前后体积的变化)
(5)将t2℃温度下pH=9的苛性钠溶液与pH=y的稀醋酸溶液等体积混合,所得混合溶液显中性,则y____3(填“大于”“小于”或“等于”);此溶液中微粒浓度的由大到小的排列顺序是________________________。(以上均忽略溶液混合前后体积的变化)
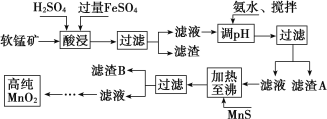
【题目】二氧化锰是制造锌锰干电池的基本材料,工业上以软锰矿、菱锰矿为原料来制备。某软锰矿主要成分为 MnO2,还含有 Si(16.27%)、Fe(5.86%)、Al(3.42%)、Zn(2.68%)和 Cu(0.86%)等元素的化合物,其处理流程图如下:
化合物 | Al(OH)3 | Fe(OH)2 | Fe(OH)3 |
Ksp 近似值 | 10-34 | 10-16 | 10-38 |
(1)硫酸亚铁在酸性条件下将 MnO2 还原为 MnSO4,酸浸时发生的主要离子反应方程式为:_____________ ;
(2)“氨水、搅拌”,其中“搅拌”不仅能加快反应速率,还能______________, 滤渣 A 的成分是 Fe(OH)3、Al(OH)3,加入氨水需调节 pH 至少达到_________________,恰好能使 Fe3+、Al3+沉淀完全(当 c≤10-5 mol·L-1 时,认为该离子沉淀完全);
(3)滤渣 B 的成分是 ________________
(4)MnO2 也可在 MnSO4-H2SO4-H2O 为体系的电解液中电解获得,其阳极反应式为:______________ 工业上采用间接氧化还原滴定法测定 MnO2 纯度,其操作过程如下:准确称量 0.920 0 g 该样品,与足量酸性 KI 溶液充分反应后,配制成 100 mL 溶液。取其中 10.00 mL,恰好与 25.00 mL 0.080 0 mol·L-1Na2S2O3溶液反应(I2 +2S 2O32-===2I-+S 4O62-)。计算可得该样品纯度为_____%(保留三位有效数字)。