题目内容
16.短周期元素X、Y、Z原子序数依次递增.X、Y、Z的最外层电子数之和为13,Y是所在周期中金属性最强的,X、Z在同一主族.(1)Z元素在周期表中的位置是第三周期第ⅥA族.
(2)X、Y、Z三种元素简单离子半径大小的顺序为Na+<O2-<S2- (用离子符号表示).
(3)Y2ZX3溶液显碱性,能证明该溶液中存在水解平衡的事实是c(填序号).
a.滴入酚酞溶液变红,再加入稀H2SO4红色退去
b.滴入酚酞溶液变红,再加入氯水红色退去
c.滴入酚酞溶液变红,再加入BaCl2溶液产生沉淀且红色退去.
分析 短周期元素X、Y、Z原子序数依次递增.Y是所在周期中金属性最强的,则Y处于ⅠA族,X、Z在同一主族,X、Y、Z的最外层电子数之和为13,令X、Z的最外层电子数为a,则a+a+1=13,解得a=6,故X为氧元素、Z为硫元素;Y的原子序数大于氧元素,则Y为Na元素.
(1)主族元素周期数=电子层数、主族族序数=最外层电子数;
(2)电子层结构相同的离子,核电荷数越大离子半径,离子的电子层越多离子半径越大;
(3)Na2SO3溶液中亚硫酸根水解,破坏水的电离平衡,溶液呈碱性;
硫酸为酸性,酚酞在酸性条件下为无色,氯水具有强氧化性,可以氧化使酚酞褪色,不能说明存在平衡.
解答 解:短周期元素X、Y、Z原子序数依次递增.Y是所在周期中金属性最强的,则Y处于ⅠA族,X、Z在同一主族,X、Y、Z的最外层电子数之和为13,令X、Z的最外层电子数为a,则a+a+1=13,解得a=6,故X为氧元素、Z为硫元素;Y的原子序数大于氧元素,则Y为Na元素,
(1)Z为硫元素,S原子核外有3个电子层,最外层电子数为6,处于周期表中第三周期第ⅥA族,故答案为:第三周期第ⅥA族;
(2)电子层结构相同的离子,核电荷数越大离子半径,离子的电子层越多离子半径越大,故离子半径为:Na+<O2-<S2-,故答案为:Na+<O2-<S2-;
(3)Na2SO3溶液中亚硫酸根水解,破坏水的电离平衡,溶液呈碱性;
硫酸为酸性,酚酞在酸性条件下为无色,氯水具有强氧化性,可以氧化使酚酞褪色,不能说明存在平衡.滴入酚酞溶液变红,说明溶液呈碱性,再加入BaCl2溶液产生沉淀,碱性减弱红色退去,说明存在平衡,故ab错误、c正确,
故答案为:碱;c.
点评 本题考查结构性质位置关系、离子半径比较、盐类水解与平衡移动等,难度不大,根据原子结构推断元素是解题关键,注意基础知识的理解掌握.

 小夫子全能检测系列答案
小夫子全能检测系列答案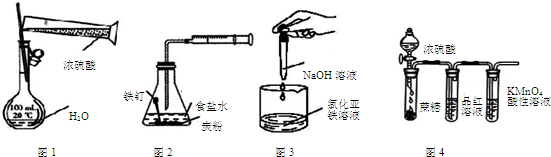
| A. | 用图1装置配制一定物质的量浓度的稀硫酸 | |
| B. | 用图2装置可探究铁的吸氧腐蚀 | |
| C. | 用图3装置可制取氢氧化亚铁 | |
| D. | 用图4装置可说明浓硫酸具有脱水性、强氧化性,SO2具有漂白性、氧化性 |
| A. | NaOH溶液[Ba(OH)2]:适量Na2SO4溶液 | B. | HNO3溶液[HCl]:过量AgNO3溶液 | ||
| C. | KOH溶液[K2CO3]:适量CaCl2溶液 | D. | Mg[Al]:过量NaOH溶液 |
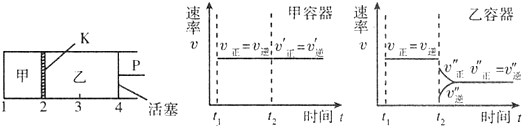
| A. | 保持温度和活塞位置不变,在甲中再加入1 mol A和2 mol B,达到新的平衡后,甲中C的浓度是乙中C的浓度的2倍 | |
| B. | 保持活塞位置不变,升高温度,达到新的平衡后,甲中B的体积分数增大,乙中B的体积分数减小 | |
| C. | 保持温度不变,移动活塞P,使乙的容积和甲相等,达到新的平衡后,乙中C的体积分数是甲中C的体积分数的2倍 | |
| D. | 保持温度和乙中的压强不变,t2时分别向甲、乙中加入等质量的氦气后,甲、乙中反应速率变化情况分别如图所示(t1前的反应速率变化已省略) |
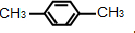 1,4-二甲苯;
1,4-二甲苯; 1,3,5-三甲苯.
1,3,5-三甲苯.
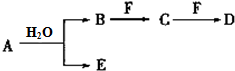 A、B、C、D、E、F为中学化学中的常见物质,且物质A由1~2种短周期元素组成,在一定条件下有如下转化关系,请完成下列问题:
A、B、C、D、E、F为中学化学中的常见物质,且物质A由1~2种短周期元素组成,在一定条件下有如下转化关系,请完成下列问题: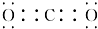 ;D中所含化学键的类型离子键、共价键.
;D中所含化学键的类型离子键、共价键.