题目内容
1.已知:通常羟基与碳碳双键相连时不稳定,易发生下列变化:
依据如下图所示的转化关系,回答问题:

(1)A的化学式是C4H6O2,官能团是酯基和碳碳双键(填名称);
(2)B的结构简式是
 ;
;(3)①的化学方程式是CH3CHO+2Cu(OH)2+NaOH△→△→CH3COONa+Cu2O↓+3H2O;
(4)F是芳香族化合物且苯环上只有一个侧链,③的化学方程式是
 ;
;(5)绿色化学中,最理想的“原子经济”是原子利用率100%,上述反应中能体现“原子经济”原则的是c(选填字母);
a.①b.③c.④d.⑤
(6)G是F的同分异构体,有关G的描述①能发生水解 ②苯环上有三个取代基 ③苯环上一溴代物有2种
据此推测G的结构简式可能是(写出其中一种)
 .
.
分析 A发生加聚反应生成B,则A的分子式为C4H6O2,A能发生酸性条件下水解反应,则A中含有酯基,A的不饱和度=4×2+2−624×2+2−62=2,结合A的分子式知,A中含有一个酯基和一个碳碳双键;
C能发生氧化反应生成D,说明C、D中碳原子个数相等,所以C、D中碳原子个数都是2,结合题给信息知,C是CH3CHO、D是CH3COOH,A是CH3COOCH=CH2,B结构简式为 ;
;
D和E发生酯化反应生成F,根据F分子式知,E分子式为C7H8O,E中不饱和度=7×2+2−827×2+2−82=4,F是芳香族化合物且苯环上只有一个侧链,所以E为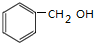 ,F为
,F为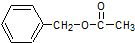 ,据此分析解答.
,据此分析解答.
解答 解:A发生加聚反应生成B,则A的分子式为C4H6O2,A能发生酸性条件下水解反应,则A中含有酯基,A的不饱和度=4×2+2−624×2+2−62=2,结合A的分子式知,A中含有一个酯基和一个碳碳双键;
C能发生氧化反应生成D,说明C、D中碳原子个数相等,所以C、D中碳原子个数都是2,结合题给信息知,C是CH3CHO、D是CH3COOH,A是CH3COOCH=CH2,B结构简式为 ;
;
D和E发生酯化反应生成F,根据F分子式知,E分子式为C7H8O,E中不饱和度=7×2+2−827×2+2−82=4,F是芳香族化合物且苯环上只有一个侧链,所以E为 ,F为
,F为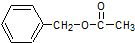 ,
,
(1)A的分子式为C4H6O2,结构简式为CH3COOCH=CH2,含有官能团是碳碳双键和酯基,
故答案为:C4H6O2;碳碳双键;
(2)通过以上分析知,B结构简式为 ,故答案为:
,故答案为: ;
;
(3)C是乙醛,乙酸和新制氢氧化铜悬浊液发生氧化反应生成乙酸钠、氧化亚铜和水,反应方程式为CH3CHO+2Cu(OH)2+NaOH△→△→CH3COONa+Cu2O↓+3H2O,
故答案为:CH3CHO+2Cu(OH)2+NaOH△→△→CH3COONa+Cu2O↓+3H2O;
(4) ,乙酸和苯甲醇在浓硫酸作催化剂、加热条件下发生酯化反应生成乙酸苯甲酯和水,反应方程式为
,乙酸和苯甲醇在浓硫酸作催化剂、加热条件下发生酯化反应生成乙酸苯甲酯和水,反应方程式为 ,
,
故答案为: ;
;
(5)体现原子经济的反应是加成或加聚反应,以上反应中只有c是加聚反应,故选c;
(6)F为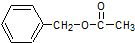 ,G是F的同分异构体,G符合下列条件:①能发生水解说明含有酯基,②苯环上有三个取代基,③苯环上一溴代物有2种说明苯环上只有两种氢原子,符合条件的同分异构体结构简式为
,G是F的同分异构体,G符合下列条件:①能发生水解说明含有酯基,②苯环上有三个取代基,③苯环上一溴代物有2种说明苯环上只有两种氢原子,符合条件的同分异构体结构简式为 ,故答案为:
,故答案为: .
.
点评 本题考查有机物推断,侧重考查学生分析推断及信息利用能力,根据分子式、反应条件结合题给信息进行推断,正确推断各物质结构简式是解本题关键,难点是同分异构体种类判断,注意C是醛而不是醇,为易错点.

| A. | 等物质的量的N2和CO所含分子数均为NA | |
| B. | 2NA个HCl分子与44.8LH2和Cl2的混合气体所含的原子数目均为4NA | |
| C. | 32gCu将浓、稀硝酸分别还原为NO2和NO,浓、稀硝酸得到的电子数均为NA | |
| D. | 常温常压下,1mol氦气含有核外电子数为4NA |
(1)工业上利用分离空气的方法得到氮气.空气各主要成分的沸点如下:
| N2 | O2 | Ar | CO2 |
| -196°C | -183°C | -186°C | -78°C |
(2)雷雨时空气中的N2转化为NO,生成物NO是无色的气体,难(填“易”或“难”)溶于水;NO在空气中很容易被氧化成NO2,NO2能与水发生化学反应.NO2与水反应的化学方程式为3NO2+H2O=2HNO3+NO.
(3)实验室可用固体NH4Cl与固体Ca(OH)2加热反应制取氨气.
①制取氨气的化学方程式为2NH4Cl+Ca(OH)2加热_加热–––––CaCl2+2H2O+2NH3↑;
②要制取标准状况下4.48L的氨气,至少需要称取固体NH4Cl的质量为10.7g.
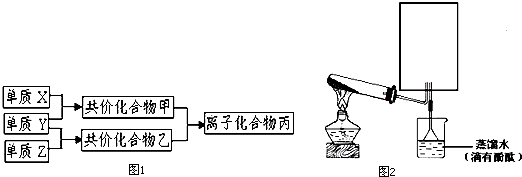
(4)已知:4NH3+6NO催化剂_催化剂–––––––5N2+6H2O.化学研究性学习小组的同学在技术人员的指导下,按下列流程,探究不同催化剂对NH3还原NO反应的催化性能.

若控制其他实验条件均相同,在催化反应器中装载不同的催化剂,将经催化反应后的混合气体,通过一定体积滴有酚酞的稀硫酸溶液(溶液的体积、浓度均相同).
①NH3与稀硫酸溶液反应的离子方程式为NH3+H+=NH4+;;
②为了比较不同催化剂的催化性能,需要测量并记录的数据是溶液显色所需时间.
| A. | 天然气的主要成分是乙烯 | |
| B. | 煤焦油分馏可以获得多种芳香烃 | |
| C. | 石油的裂化和裂解都属于物理变化 | |
| D. | 天然气、沼气都属于可再生的清洁能源 |
| A. | CH4O | B. | C2H4O | C. | C2H6O | D. | C2H6O2 |
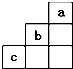
| A. | b的氢化物很稳定 | |
| B. | a是一种活泼的非金属元素 | |
| C. | c的最高价氧化物的水化物是一种弱酸 | |
| D. | b元素在化合物中的最高价为+7价 |
| A. | 0.5L0.1mol/L的NaCl溶液 | B. | 1L0.2mol/L的MgCl2溶液 | ||
| C. | 1L0.3mol/L盐酸溶液 | D. | 100mL0.2mol/L的AlCl3溶液 |
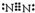 .
.