题目内容
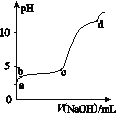
【题目】常温下,将一定量的钠铝合金置于水中,合金全部溶解,得到20 mL pH=14的溶液,然后用1 mol/L的盐酸滴定,测得生成沉淀的质量与消耗盐酸的体积关系如图所示,则下列说法正确的是( )

A. 原合金质量为 0.92 g
B. 产生氧气的体积为896 mL(标准状况下)
C. 图中m的值为1.56
D. 图中V2的值为60
【答案】C
【解析】试题分析:反应后得到20 mL pH=14的溶液,所以n(OH-)=0.02mol,所以需要1mol/L的盐酸20mL来中和,因此V1为20mL,继续加盐酸发生AlO2-+H++H2O=Al(OH)3,Al(OH)3+3H+=Al3++3H2O,因此沉淀AlO2-用掉20mL盐酸,溶解Al(OH)3用掉60mL盐酸,所以V2为100mL。所以Al(OH)3为0.02mol,则m为1.56g,原混合物中含有Al为0.54g,当盐酸加100mL时,溶液中的溶质为NaCl和AlCl3,又知n(Cl-)=0.1mol,n(Al3+)=0.02mol,所以n(Na+)=0.04mol。所以原混合物中有Na为0.04mol,质量为0.92g,所以原混合物的质量为0.92g+0.54g=1.46g。反应过程中产生氢气0.05mol,1120mL,则C正确;答案选C。

 名校课堂系列答案
名校课堂系列答案【题目】一定温度下,在三个体积均为2 L的恒容密闭容器中发生反应:CO2(g)+H2S(g)![]() COS(g)+H2O(g)。
COS(g)+H2O(g)。
容器 | 温度/K | 起始物质的量/mol | 平衡物质的量/mol | 平衡常数 | |
CO2 | H2S | H2O | |||
I | 607 | 0.1 | 0.15 | 0.05 | |
Ⅱ | 607 | 0.2 | 0.3 | ||
Ⅲ | 627 | 0.1 | 0.15 | 6×l0-3 | |
下列说法正确的是
A. 该反应为吸热反应
B. 容器Ⅲ达到平衡时,再充入少量氦气,平衡将向正反应方向移动
C. 容器Ⅱ达到平衡时,容器中COS的物质的量浓度为0.025 mol L-1
D. 607 K时,该反应的平衡常数为0.50