题目内容
【题目】室温下,在0.2 mol·L-1 Al2(SO4)3溶液中,逐滴加入1.0 mol·L-1 NaOH溶液,实验测得溶液pH随NaOH溶液体积的变化曲线如图所示,下列有关说法正确的是( )
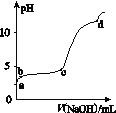
A. a点时,溶液呈酸性的原因是Al3+水解,离子方程式为Al3++3OH-![]() Al(OH)3
Al(OH)3
B. a~b段,溶液pH增大,Al3+浓度不变
C. b~c段,加入的OH-主要用于生成Al(OH)3沉淀
D. d点时,Al(OH)3沉淀开始溶解
【答案】C
【解析】试题分析:A.a点溶液是Al2(SO4)3,,溶液呈酸性的原因是Al3+水解,Al3+水解消耗水电离产生的OH-,破坏了水的电离平衡,水会继续电离,当最终达到平衡时,由于c(H+)>c(OH-),所以溶液显碱性,离子方程式为:Al3++3H2O![]() Al(OH)3+3H+,错误;B.a~b段,随着NaOH溶液的不断滴入,OH-会中和水解产生的H+,使盐的水解程度增大,所以溶液中Al3+浓度减小,而溶液的pH增大,错误;C.b~c段,加入的OH-主要用于生成Al(OH)3沉淀,正确;D.在d点时,NaOH过量,溶液是NaAlO2和NaOH的混合溶液,错误;故答案选C。
Al(OH)3+3H+,错误;B.a~b段,随着NaOH溶液的不断滴入,OH-会中和水解产生的H+,使盐的水解程度增大,所以溶液中Al3+浓度减小,而溶液的pH增大,错误;C.b~c段,加入的OH-主要用于生成Al(OH)3沉淀,正确;D.在d点时,NaOH过量,溶液是NaAlO2和NaOH的混合溶液,错误;故答案选C。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目