��Ŀ����
����Ŀ��������һ����Ҫ�Ļ�����Ʒ���й㷺��;����ҵ�Ͽ����������͵����ϳɡ�
(1)��֪����:N![]() N 945kJ��mol-1��H-H 436 kJ��mol-1��N-H 391kJ��mol-1��
N 945kJ��mol-1��H-H 436 kJ��mol-1��N-H 391kJ��mol-1��
�ٵ����������ϳɰ����Ȼ�ѧ����ʽ��______________��
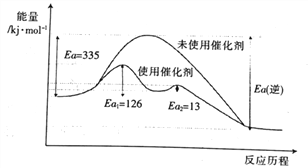
��δʹ�ô���ʱ���淴Ӧ�Ļ��Ea(��)=______ kJ��mol-1��ʹ�ô���֮������Ӧ���ܻ��Ϊ_______ kJ��mol-1��
(2)�±��ǵ���Ӧ���а�n(N2):n(H2)=l:3Ͷ�Ϻ���200�桢400�桢600�棬��Ӧ�ﵽƽ��ʱ���������NH3�����ʵ�����������ѹǿ�ı仯���ߡ�

������a��b��Ӧ�¶Ƚϸߵ���________ (����a������b��)
��ʵ����ģ�ҵ�ϳɰ���һ���¶Ⱥ�ѹǿ����1L�ܱ�������ͨ��5 mol N2��15molH2��10min ��ﵽM��ƽ��״̬������ӷ�Ӧ��ʼ��ƽ��ʱ����ڵ�ƽ������V(N2)___mol��L-1��min-1��
�۹��ڹ�ҵ�ϳɰ��ķ�Ӧ������������ȷ����_______(����ĸ)��
A.�����NH3���ԭ����ѭ�����ã��������H2��ƽ��ת����
B.ʹ�ݴ����ܼӿ췴Ӧ���������H2��ƽ��ת����
C.��ͼ��M��Q��R��ƽ�ⳣ��K�Ĵ�С��ϵ��K(M)= K(Q)> K(R)
���г�R��ƽ�ⳣ���ļ���ʽKp=____(MPa)-2������ƽ���ѹ����ƽ��Ũ�ȼ��룬��ѹ=��ѹ�����ʵ�����������Ҫ���������
���𰸡� N2(g) + 3H2(g) ![]() 2NH3(g) ��H= -93 kJ��mol-1 428 126 b 0.375 AC
2NH3(g) ��H= -93 kJ��mol-1 428 126 b 0.375 AC 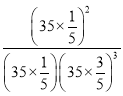 �����������𰸶����֣�
�����������𰸶����֣�
��������(1)����֪���ܣ�N![]() N 945kJ��mol-1��H-H 436 kJ��mol-1��N-H 391kJ��mol-1����N2(g) + 3H2(g)
N 945kJ��mol-1��H-H 436 kJ��mol-1��N-H 391kJ��mol-1����N2(g) + 3H2(g) ![]() 2NH3(g) ��H=��945kJ��mol-1+3��436 kJ��mol-1��-��6��391kJ��mol-1��= -93 kJ��mol-1���ʵ����������ϳɰ����Ȼ�ѧ����ʽ��N2(g) + 3H2(g)
2NH3(g) ��H=��945kJ��mol-1+3��436 kJ��mol-1��-��6��391kJ��mol-1��= -93 kJ��mol-1���ʵ����������ϳɰ����Ȼ�ѧ����ʽ��N2(g) + 3H2(g) ![]() 2NH3(g) ��H= -93 kJ��mol-1��
2NH3(g) ��H= -93 kJ��mol-1��
��δʹ�ô���ʱ���淴Ӧ�Ļ��Ea(��)=��335+93��kJ��mol-1=428kJ��mol-1��ʹ�ô���֮������Ӧ���ܻ��ΪEa1=126kJ��mol-1��
(2)���ϳɰ�������Ϊ���ȷ�Ӧ�������¶�ƽ�������ƶ���NH3�����ʵ���������С��������a��b��Ӧ�¶Ƚϸߵ���b��
��M��NH3�����ʵ�������Ϊ60%��
N2(g) + 3H2(g) ![]() 2NH3(g)
2NH3(g)
��ʼ���ʵ���Ũ�ȣ�mol/L�� 5 15 0
�仯���ʵ���Ũ�ȣ�mol/L�� n 3n 2n
��ʼ���ʵ���Ũ�ȣ�mol/L�� 5-n 15-3n 2n
NH3�����ʵ�������Ϊ60%=![]() ��100%����ã�n=
��100%����ã�n=![]() ����ӷ�Ӧ��ʼ��ƽ��ʱ����ڵ�ƽ������V(N2)=
����ӷ�Ӧ��ʼ��ƽ��ʱ����ڵ�ƽ������V(N2)= ![]() =0.375mol��L-1��min-1��
=0.375mol��L-1��min-1��
��A����ʱ�����NH3����ѭ������ԭ�������������H2��ƽ��ת���ʣ���A��ȷ��B��ʹ�ݴ����ܼӿ췴Ӧ���ʣ�����Ӱ��ƽ����ƶ�����H2��ת������Ӱ�죬��B����C��ƽ�ⳣ�����¶��йأ������������أ��¶���ͬʱƽ�ⳣ����ͬ����Ӧ�Ƿ��ȷ�Ӧ���¶�Խ��ƽ�ⳣ��ԽС����M��Q��R��ƽ�ⳣ��K�Ĵ�С��ϵ��K��M��=K��Q����K��R������C��ȷ����ΪAC��
��R����ѹǿΪ35MPa��NH3�����ʵ�������Ϊ20%��
N2(g) + 3H2(g) ![]() 2NH3(g)
2NH3(g)
��ʼ���ʵ�����mol�� 5 15 0
�仯���ʵ�����mol�� n 3n 2n
��ʼ���ʵ�����mol�� 5-n 15-3n 2n
NH3�����ʵ�������Ϊ20%=![]() ��100%����ã�n=
��100%����ã�n=![]() ����N2�����ʵ�������Ϊ
����N2�����ʵ�������Ϊ![]() ��100%=
��100%=![]() ��H2�����ʵ�������Ϊ1-
��H2�����ʵ�������Ϊ1- ![]() -
- ![]() =
=![]() ��R��ƽ�ⳣ���ļ���ʽKp=
��R��ƽ�ⳣ���ļ���ʽKp=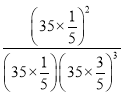 (MPa)-2��
(MPa)-2��

����Ŀ��A��B��C��D��E��F���ֶ�����Ԫ��,���ǵ�ԭ��������������,A��Dͬ���壻C��Eͬ���壻B��Cͬ���ڣ�Bԭ���������������������������2��A�����ڱ��а뾶��С��Ԫ��,C���������������ڲ���ӵ�3����FԪ����ͬ����Ԫ����ԭ�Ӱ뾶��С������Ԫ�ء�A��B��C��D��E�γɵĻ�����ס��ҡ�����������������ʾ��
������ | �� | �� | �� | �� |
��ѧʽ | A2C | A2C2 | D2C2 | D2E |
�ش���������:
(1)ָ��Ԫ��F�����ڱ��е�λ��___________��
(2)��������ĵ���ʽΪ__________,�õ���ʽ��ʾ�γɻ����ﶡ�Ĺ���_______��
(3) ����Һ�м��������ữ������Һ��д����Ӧ�����ӷ���ʽ:_______��
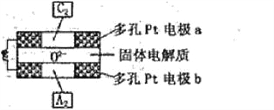
(4)����������ȼ�ϵ�����Թ��������һ������Ϊ����ʣ����ֹ��������ڸ���������02-�����ͨ�����õ�صĹ���ԭ����ͼ��ʾ�����ж��Pt�缫a��b�ֱ�������C2��A2�����塣�õ�ص�����Ϊ______ (��a��b)��02-����______������������������õ�صĸ�����ӦΪ _________ ��