题目内容
下列溶液中有关物质的量浓度关系和计算不正确的是 ( )
A.pH相等的NaOH、CH3COONa和NaHCO3三种溶液,则有c(NaOH)<c(NaHCO3)
<c(CH3COONa)
B.已知25°C时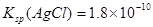 ,则在0.1mol·L-1AlCl3溶液中,Ag+的物质
,则在0.1mol·L-1AlCl3溶液中,Ag+的物质
的量浓度最大可达到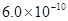 mol·L-1
mol·L-1
C.25°时,0.1mol·L-1Na2CO3溶液中水电离出来的OH-浓度大于0.1mol·L-1NaOH溶
液中水电离出来的OH-浓度
D.室温下,0.1mol·L-1NaHA溶液的pH=4,则有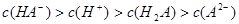
【答案】
D
【解析】选项D,HA-是弱电解质离子,且HA-的电离大于水解,故应该是c(A2-)>c(H2A)。选项A,当pH相等时,原来碱性强的物质,浓度反而小;原来碱性弱的物质,浓度反而大;故选项A正确。选项B,根据c(Ag+)·c(C1—)=Ksp=1.8×10 -10,将c(Cl-)=0.3 mol.L-l代入式中计算即可。选项C,Na2CO3水解,促进水电离,NaOH是碱,抑制水电离。

练习册系列答案
相关题目
下列溶液中有关物质的浓度关系正确的是( )
| A、c(NH4+)相等的(NH4)2SO4、NH4HSO4、NH4Cl溶液中:c(NH4HSO4)>c[(NH4)2SO4]>c(NH4Cl) | B、向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) | C、1.0 mol/L Na2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3) | D、某二元弱酸的酸式盐NaHA溶液中:c(H+)+c(Na+)=c(OH-)+c(HA-)+c(A2-) |