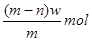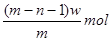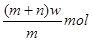题目内容
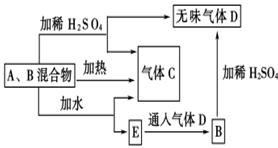
(12分)已知:A、B、C为中学常见的单质,A为淡黄色固体;D、E、F为中学常见的氧化物,E是具有磁性的黑色晶体;H、K为中学常见的盐;M为一种常见的无色液体。各物质间的转化关系如下图所示(某些条件已略去)。

请回答:
(1)物质K的化学式为 。
(2)物质M的电子式为 。
(3)D可使酸性KMnO4溶液褪色,体现了D物质的 (填字母序号)。
A. 氧化性 B. 还原性 C. 漂白性
(4)C与M在一定条件下反应的化学方程式为 。
(5)先将D气体通入BaCl2溶液中,再通入NH3,实验过程中的现象为 。
(6)H溶液在空气中常期放置会出现红褐色浑浊,请用一个离子方程式表示其变化的原因: 。
(7)A与C可以在一定条件下发生化合反应,其产物中元素A与C的质量比为4:7,该物质是某矿石的主要成分之一,常用于生产G。某化工厂所用矿石样品含杂质25%,若取8.8吨该矿石,假设生产过程中无其他损失,可制得含G 98%的产品 吨。

请回答:
(1)物质K的化学式为 。
(2)物质M的电子式为 。
(3)D可使酸性KMnO4溶液褪色,体现了D物质的 (填字母序号)。
A. 氧化性 B. 还原性 C. 漂白性
(4)C与M在一定条件下反应的化学方程式为 。
(5)先将D气体通入BaCl2溶液中,再通入NH3,实验过程中的现象为 。
(6)H溶液在空气中常期放置会出现红褐色浑浊,请用一个离子方程式表示其变化的原因: 。
(7)A与C可以在一定条件下发生化合反应,其产物中元素A与C的质量比为4:7,该物质是某矿石的主要成分之一,常用于生产G。某化工厂所用矿石样品含杂质25%,若取8.8吨该矿石,假设生产过程中无其他损失,可制得含G 98%的产品 吨。
(12分)
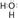
(1)Fe2(SO4)3
(2) (2分)
(3) B(4) 3Fe + 4H2O(g) === Fe3O4 + 4H2 (2分)(反应条件写“高温”或“加热”均可)
(5)先无明显现象,通入NH3后产生白色沉 淀 (各1分,共2分)
淀 (各1分,共2分)
(6) 4Fe2+ + O2 + 10H2O ="==" 4Fe(OH)3 + 8H+ (2分)
(该反应产物不唯一,答案合理均可给分)
(7)7.5 (2分)
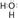
(1)Fe2(SO4)3
(2) (2分)
|
(5)先无明显现象,通入NH3后产生白色沉
 淀 (各1分,共2分)
淀 (各1分,共2分)(6) 4Fe2+ + O2 + 10H2O ="==" 4Fe(OH)3 + 8H+ (2分)
(该反应产物不唯一,答案合理均可给分)
(7)7.5 (2分)
略

练习册系列答案
相关题目