题目内容
某温度下的溶液中c(H+)=10xmol/L,c(OH-)=10ymol/L。x与y的关系图所示,下列说法正确的是
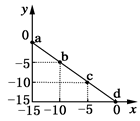

| A.该温度高于25℃ |
| B.图中a点溶液呈碱性 |
| C.该温度下,0.01 mol·L-1的HCl溶液的pH=2 |
| D.该温度下,0.01 mol·L-1的NaOH溶液的pH=12 |
BC
试题分析:A、c(OH-)+c(H+)=10-15,而25°时c(OH-)+c(H+)=10-14,故该温度应低于25℃。
B、a点对应的c(H+)=10—15mol/L,c(OH-)=0mol/L,故为碱性。
C、0.01 mol·L-1的HCl溶液中c(H+)=10-2,根据pH=-㏒10(H+),得PH=2。
点评:此题考核了溶液PH和氢离子、氢氧根离子的关系,熟悉掌握PH的计算式,难度不大。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
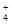 )与c(SO
)与c(SO )之比是 ( )
)之比是 ( )