题目内容
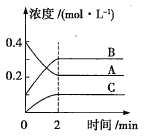
【题目】如图所示为800℃时A、B、C三种气体在密闭容器中反应时的浓度变化情况,则下列说法错误的是( )

A.发生的反应可表示为2A(g)![]() 3B(g)+C(g)
3B(g)+C(g)
B.前2min,A的分解速率为0.1mol·L-1·min-1
C.2min后反应达到平衡状态
D.2min时,A、B、C的浓度之比为2:3:1
【答案】A
【解析】
A.根据图象可知,反应过程中A的浓度减小,B、C的浓度增大,因此A为反应物,B、C为生成物,根据浓度的变化量可以确定反应为![]() ,故A错误;
,故A错误;
B.前2min,![]() ,故B正确;
,故B正确;
C.2min后A、B、C的浓度不再变化,反应达到平衡状态,故C正确;
D.据图可知2min时,A、B、C的浓度分别为0.2mol/L、0.3mol/L 、0.1mol/L,比值为2:3:1,故D正确;
故答案为A。

 阅读快车系列答案
阅读快车系列答案【题目】下表是几种常见弱酸的电离平衡常数(25℃ )
化学式 | H2CO3 | CH3COOH | HClO |
电离平衡常数 | K1=4.3×10-7 K2=5.6×10-11 | 1.8×10-5 | 3.0×10-8 |
(1)根据分析表格中数据可知,H2CO3、CH3COOH、HClO三种酸的酸性从强到弱依次是_____________________________________。
(2)常温下,0.1molL﹣1 CH3COOH溶液加水稀释过程中,下列表达式的数据变大的是_________(填字母)
A.c(H+)B.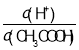 C.c(H+)c(OH﹣)D.
C.c(H+)c(OH﹣)D.![]() E.
E.![]()
(3)25℃时,等浓度的Na2CO3、CH3COONa和NaClO三种溶液的pH从小到大依次是_____________________________________。
(4)25℃时,将a molL﹣1的醋酸与b molL﹣1氢氧化钠等体积混合,反应后溶液恰好显中性,溶液中离子浓度大小关系:_________________
(5)下列反应不能发生的是______(填字母)。
a.![]() +2CH3COOH=2CH3COO-+CO2↑+H2O b.ClO-+CH3COOH=CH3COO-+HClO
+2CH3COOH=2CH3COO-+CO2↑+H2O b.ClO-+CH3COOH=CH3COO-+HClO
c.![]() +2HClO=CO2↑+H2O+2ClO- d.2ClO-+CO2+H2O=
+2HClO=CO2↑+H2O+2ClO- d.2ClO-+CO2+H2O=![]() +2HClO
+2HClO