题目内容
【题目】短周期元素X、Y、Z组成的化合物Y2X和ZX2。Y2X溶于水形成的溶液能与ZX2反应生成一种化合物Y2ZX3.已知三种元素原子的质子总数为25,且Z和Y的原子序数之和比X的原子序数2倍还多1,Z原子有2个电子层,最外层电子数是核外电子数的2/3倍,试回答:
(1)X元素的名称:_______,Y元素在元素周期表中的位置_____________,Z元素的原子结构示意图____________。
(2)Y2X对应水化物的电子式____________,其中存在的化学键有____________。
(3)X的氢化物比同主族的氢化物的熔沸点明显偏高的原因___________________。
(4)用电子式表示Y2X的形成过程:________________________________________
【答案】 氧 第三周期IA族 ![]()
![]() 离子键、共价键 H2O分子之间存在氢键
离子键、共价键 H2O分子之间存在氢键 ![]()
【解析】Z原子有2个电子层,最外层电子数是核外电子数的2/3倍,令最外层电子数为a,则2/3(2+a)=a,解得a=4,所以Z为C元素;设X原子的质子数为x,Y原子的质子数为y,三种元素原子的质子总数为25,则有6+x+y=25,Z和Y的原子序数之和比X的原子序数2倍还多1,则有6+y=2x+1,联立方程解得:x=8,y=11,即X为氧元素,Y为钠元素。
(1)由上述分析可知,X为氧元素,Y为钠元素,处于周期表中第三周期第IA族,Z为碳元素,原子结构示意图为: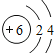 。(2)Y2X为Na2O,对应水化物为NaOH,其电子式为:
。(2)Y2X为Na2O,对应水化物为NaOH,其电子式为:![]() ,含有离子键、共价键。(3)H2O分子之间存在氢键,因此比同主族的氢化物的熔沸点明显偏高。(4)氧化钠是离子化合物,用电子式表示Na2O的形成过程为
,含有离子键、共价键。(3)H2O分子之间存在氢键,因此比同主族的氢化物的熔沸点明显偏高。(4)氧化钠是离子化合物,用电子式表示Na2O的形成过程为![]() 。
。

 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案【题目】新型电池在飞速发展的信息技术中发挥着越来越重要的作用。Li2FeSiO4是极具发展潜力的新型锂离子电池电极材料,在苹果的几款最新型的产品中已经有了一定程度的应用。其中一种制备Li2FeSiO4的方法为:固相法:2Li2SiO3+FeSO4![]() Li2FeSiO4+Li2SO4+SiO2
Li2FeSiO4+Li2SO4+SiO2
某学习小组按如下实验流程制备Li2FeSiO4并测定所得产品中Li2FeSiO4的含量。
实验(一)制备流程:
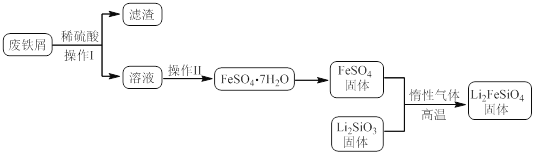
实验(二) Li2FeSiO4含量测定:
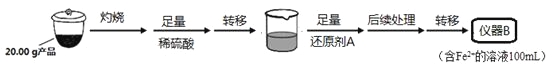
从仪器B中取20.00 mL溶液至锥形瓶中,另取0.2000 mol·Lˉ1的酸性KMnO4标准溶液装入仪器C中,用氧化还原滴定法测定Fe2+含量。相关反应为:MnO4- +5Fe2++8H+=Mn2++5Fe3++4H2O,杂质不与酸性KMnO4标准溶液反应。经4次滴定,每次消耗KMnO4溶液的体积如下:
实验序号 | 1 | 2 | 3 | 4 |
消耗KMnO4溶液体积 | 20.00 mL | 19.98mL | 21.38mL | 20.02mL |
(1)实验(二)中的仪器名称:仪器B ,仪器C 。
(2)制备Li2FeSiO4时必须在惰性气体氛围中进行,其原因是 。
(3)操作Ⅱ的步骤 ,在操作Ⅰ时,所需用到的玻璃仪器中,除了普通漏斗、烧杯外,还需 。
(4)还原剂A可用SO2,写出该反应的离子方程式 ,此时后续处理的主要目的是 。
(5)滴定终点时现象为 ;根据滴定结果,可确定产品中Li2FeSiO4的质量分数为 ;若滴定前滴定管尖嘴处有气泡,滴定后消失,会使测得的Li2FeSiO4含量 。(填“偏高”、“偏低”或“不变”)。