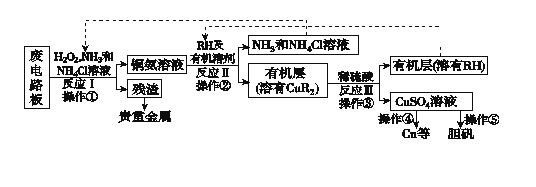
题目内容
【题目】下列关于四个实验装置的说法中正确的是( )


A. 图一:引发铝热反应的操作是点燃镁条
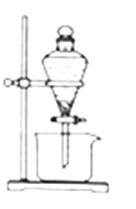
B. 图二:海水淡化的蒸馏操作中缺少了温度计
C. 图三:滴加K3[Fe(CN)6]溶液,产生特征蓝色沉淀
D. 图四:酸式滴定管注入Na2CO3溶液之前应检查是否漏液
【答案】A
【解析】A. 铝热反应的引发就是点燃镁条;B蒸馏操作需要温度计,通过控制蒸气温度来判断蒸出物,但海水淡化不需要温度计,只要收集蒸气即可;C.该装置为原电池,锌活泼作负极,H+作氧化剂在铁电极上放电,故原电池开始工作后铁电极不参加反应,加K3[Fe(CN)6]溶液不会产生特征蓝色沉淀;D项,碳酸钠溶液呈碱性不能注入酸式滴定管。
详解:A.点燃Mg条,引发反应,可引发铝热反应,所以A选项是正确的;
B. 蒸馏操作需要温度计,通过控制蒸气温度来判断蒸出物,但海水淡化不需要温度计,只要收集蒸气即可,故B错误;
C. 该装置为原电池,锌活泼作负极,H+作氧化剂在铁电极上放电,故原电池开始工作后铁电极不参加反应,加K3[Fe(CN)6]溶液不会产生特征蓝色沉淀,故C错误;
D. 碳酸钠溶液呈碱性不能注入酸式滴定管,故D错误。
所以A选项是正确的。

 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案【题目】下表是元素周期表的一部分
族 周期 | |||||||
① | |||||||
Li | C | ④ | ⑤ | ⑥ | |||
⑦ | ⑧ | ⑨ | ⑩ | ||||
K | ⑾ | ||||||
(1)表中元素______的非金属性最强(填写元素符号,下同);元素______的单质室温下呈液态,它的原子序数是__________
(2)表中元素⑤和⑦、①和⑤均可以组成原子比例为1:1的物质,这两种物质内所含有的相同的化学键是________键(填写“离子键”、“极性共价键”或“非极性共价键”);表中元素⑥⑩⑾氢化物的稳定性由大到小的顺序为:____________________(填写化学式,下同;
(3)表中有一种元素的单质可作为半导体材料,它在元素周期表中的位置是____________;用电子式表示表中⑧⑩两元素形成化合物的过程____________。