题目内容
【题目】黑火药爆炸时发生多种化学反应,其中主要化学反应方程式为:
2KNO3+3C+S ![]() K2S+N2↑+3CO2↑
K2S+N2↑+3CO2↑
(1)上述反应中,原子半径最小的元素其原子结构示意图为 .
(2)写出上述反应生成物中,属于非电解质的物质的电子式 , 属于电解质的物质的电子式 .
(3)上述反应中,每生成1mol氧化产物,消耗KNO3的质量为(保留1位小数).
(4)黑火药爆炸后气体产物中有一种能造成酸雨的物质,它与酸性高锰酸钾溶液反应,能使溶液生成Mn2+而使紫红色退去.
①气体产物与酸性高锰酸钾溶液反应的离子方程式 .
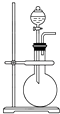
②利用如图装置检验气体产物中的CO气体,一段时间后,观察到B中出现黑色的Pd沉淀,写出B中发生反应的化学方程式 . 
【答案】
(1)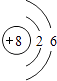
(2)CO2;K2S
(3)67.3
(4)5SO2+2MnO4﹣+2H2O=5SO42﹣+2Mn2++4H+;CO+PdCl2+H2O=Pd+2HCl+CO2
【解析】解:(1)根据元素周期律知,原子半径最小的元素是O元素,其原子结构示意图为 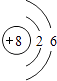 ,所以答案是:
,所以答案是: 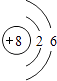 ;(2)在水溶液里和熔融状态下不导电的化合物是非电解质,在水溶液里或熔融状态下导电的化合物是电解质,所以上述物质中属于非电解质的是CO2 , 属于电解质的是
;(2)在水溶液里和熔融状态下不导电的化合物是非电解质,在水溶液里或熔融状态下导电的化合物是电解质,所以上述物质中属于非电解质的是CO2 , 属于电解质的是
K2S;所以答案是:CO2;K2S;(3)该反应中,N元素化合价由+5价变为0价、C元素化合价由0价变为+4价、S元素化合价由0价变为﹣2价,所以氧化产物是二氧化碳,根据二氧化碳和硝酸钾之间的关系式得,硝酸钾的质量= ![]() ×2×101g/mol=67.3g,所以答案是:67.3g;(4)收集黑火药爆炸后的烟尘和气体产物,分别与酸性高锰酸钾溶液反应,均能使溶液紫红色退去,说明其烟尘和气体中含有还原性物质,①二氧化硫具有还原性,能被酸性高锰酸钾溶液氧化生成硫酸根离子,高锰酸根离子被还原生成镁离子,离子方程式为5SO2+2MnO4﹣+2H2O=5SO42﹣+2Mn2++4H+ , 所以答案是:5SO2+2MnO4﹣+2H2O=5SO42﹣+2Mn2++4H+;②利用图装置检验气体产物中的CO气体,一段时间后,观察到B中出现黑色的Pd沉淀,说明CO和氯化铅发生反应生成Pb,CO被氧化生成二氧化碳,再结合原子守恒知,反应物还有水、生成物还有HCl,所以反应方程式为CO+PdCl2+H2O=Pd+2HCl+CO2 ,
×2×101g/mol=67.3g,所以答案是:67.3g;(4)收集黑火药爆炸后的烟尘和气体产物,分别与酸性高锰酸钾溶液反应,均能使溶液紫红色退去,说明其烟尘和气体中含有还原性物质,①二氧化硫具有还原性,能被酸性高锰酸钾溶液氧化生成硫酸根离子,高锰酸根离子被还原生成镁离子,离子方程式为5SO2+2MnO4﹣+2H2O=5SO42﹣+2Mn2++4H+ , 所以答案是:5SO2+2MnO4﹣+2H2O=5SO42﹣+2Mn2++4H+;②利用图装置检验气体产物中的CO气体,一段时间后,观察到B中出现黑色的Pd沉淀,说明CO和氯化铅发生反应生成Pb,CO被氧化生成二氧化碳,再结合原子守恒知,反应物还有水、生成物还有HCl,所以反应方程式为CO+PdCl2+H2O=Pd+2HCl+CO2 ,
所以答案是:CO+PdCl2+H2O=Pd+2HCl+CO2 .

 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案【题目】下表是周期表中的一部分,根据①﹣⑩在周期表中的位置,用元素符号或化学式回答下列问题:
族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
1 | ① | |||||||
2 | ④ | ⑦ | ⑧ | ⑩ | ||||
3 | ② | ③ | ⑤ | ⑥ | ⑨ |
(1)表中元素,化学性质最不活泼的是 , 只有负价而无正价的是 , 还原性最强的单质是 , 可用于制半导体材料的元素是;
(2)最高价氧化物的水化物酸性最强的是 , 呈两性的是 , 最高价氧化物的水化物碱性最强的是 , 电子式为;
(3)在②、③、④、⑤、⑥、⑦、⑧、⑨中,原子半径最大的是;
(4)比较⑥⑦⑨氢化物的稳定性最弱的是;
(5)③元素单质和②元素最高价氧化物对应的水化物相互反应的离子方程式为;
(6)铍(Be)位于元素周期表中第二周期第ⅡA族.相同条件下,单质铍与酸反应比单质锂与酸反应更加(填“剧烈”或“缓慢”),写出铍与盐酸反应的化学方程式 .