题目内容
【题目】工业合成氨的反应为:N2(g) + 3H 2(g) ![]() 2NH3(g); △H<0
2NH3(g); △H<0
(1)、随着温度升高,平衡常数K值变_______。
(2)改变反应条件,会使平衡发生移动。如下图像表示随条件改变,氨气的百分含量的变化趋势。

当横坐标为压强时,变化趋势正确的是(选填字母序号)_________,
当横坐标为温度时,变化趋势正确的是(选填字母序号)__________。
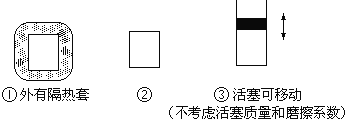
(3)如图所示三个容积相同的容器①、②、③,若起始温度相同,分别向三个容器中充入①中3mol H2和1mol N2;②中2mol NH3;③中1.5mol H2和0.5mol N2和1mol NH3;一定条件下反应,达到平衡时各容器中NH3物质的百分含量由大到小的顺序为_____(填容器编号)。
(4)氨气和氧气从145℃就开始反应,在不同温度和催化剂条件下生成不同产物(如图所示):
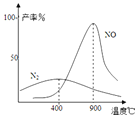
4NH3+5O24NO+6H2O 4NH3+3O22N2+6H2O 温度高于900℃时,NO产率下降的原因_____。
【答案】 减小 b a ①<②<③ 高温生成NO,放热,温度高于900℃产率下降
【解析】(1)合成氨反应是放热反应,温度升高,平衡逆向移动,c(NH3)减小,c(N2)、c(H2)增大,所以平衡常数减小;(2)当横坐标为压强时,因为增大压强,平衡正向移动,NH3含量增大,变化趋势正确的是b,当横坐标为温度时,因为反应正向放热,升温,平衡逆向移动,NH3含量降低,变化趋势正确的是a;
(3)③恒温、恒压;充入3mol H2和1mol N2 ,反应正向进行,气体总量减小,体积收缩;②恒温、恒容,相当于在③的基础上进行减压操作,平衡将向逆向移动氨的百分含量相对应于③是下降的!即②<③;①恒容,外有隔热套,反应进行,反应放热,相当于在②的基础上进行加热操作,平衡将向逆向移动,氨的百分含量下降;即①<②。故答案为①<②<③;(4)由图象可知在温度较低时生成氮气.温度高于900℃时,NO产率下降是因为反应4NH3+5O2![]() 4NO+6H2O是放热反应,达到平衡后,升温平衡逆向进行。故产率降低.吸收塔中需要补充空气是增加反应物的浓度,使平衡向正向移动,进一步与NO反应生成硝酸。
4NO+6H2O是放热反应,达到平衡后,升温平衡逆向进行。故产率降低.吸收塔中需要补充空气是增加反应物的浓度,使平衡向正向移动,进一步与NO反应生成硝酸。

 智慧小复习系列答案
智慧小复习系列答案【题目】室温下,有关下列四种溶液的叙述正确的是(忽略溶液混合的体积变化)
① | ② | ③ | ④ | |
pH | 12 | 12 | 2 | 2 |
溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
A. 在①、②中分别加入氯化铵晶体,两溶液的pH值均增大
B. 分别将等体积的①和②加水稀释100倍,所得溶液的pH:①>②
C. 把①、④两溶液等体积混合后所得溶液显酸性
D. 将溶液②和溶液③等体积混合,混合后所得溶液pH=7