题目内容
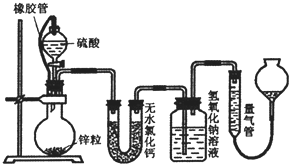 不同浓度的硫酸与锌反应时,硫酸可以被还原为S02,也可被还原为氢气.某校研究性学习小组拟设计实验验证这一事实,并进行数据测定和相关计算.
不同浓度的硫酸与锌反应时,硫酸可以被还原为S02,也可被还原为氢气.某校研究性学习小组拟设计实验验证这一事实,并进行数据测定和相关计算.(1)该小组设计了如图所示的实验装置,检查该装置气密性的操作是
(2)若在烧瓶中放入1.30g锌粒,与c mol?L-1H2SO4,反应.为保证实验结论的可靠,量气管的适宜规格是(填字母)
A.100mL B.200mL C.400mL D.500mL
(3)若1.30g锌粒完全溶解.氢氧化钠洗气瓶增重0.64g(烧瓶中残留气体忽略不计,下同).则圆底烧瓶中发生反应的化学方程式为
(4)若烧瓶中投入a g锌且完全反应,氢氧化钠洗气瓶增重b g,量气管中收集到V mL气体(标准状况),请用一个代数式表示出a、b、V之间的关系
(5)若撤走盛有无水氯化钙的U型管,则n(H2)/n(SO2)的数值将
(6)反应结束后,为了准确地测量气体体积,读数时应注意的事项是
分析:(1)可关闭分液漏斗活塞,向右侧球形管中加入水,观察液面是否发生变化;
(2)n(Zn)=0.02mol,理论生成n(H2)=0.02mol,v(H2)=0.02mol×22.4L/mol=0.448L=448mL,以此选择量气管的适宜规格;
(3)如发生Zn+2H2SO4=ZnSO4+SO2↑+2H2On(Zn)=0.02mol,应生成n(SO2)=
=0.01mol,小于0.02mol,说明还有氢气生成;
(4)根据反应的方程式Zn+2H2SO4=ZnSO4+SO2↑+2H2O、Zn+H2SO4=ZnSO4+H2↑计算,n(Zn)=n(SO2)+n(H2);
(5)若撤走盛有无水氯化钙的U型管,则氢氧化钠洗气瓶增重偏大;
(6)为了准确地测量气体体积,读数时应注意气体温度、压强等问题的影响.
(2)n(Zn)=0.02mol,理论生成n(H2)=0.02mol,v(H2)=0.02mol×22.4L/mol=0.448L=448mL,以此选择量气管的适宜规格;
(3)如发生Zn+2H2SO4=ZnSO4+SO2↑+2H2On(Zn)=0.02mol,应生成n(SO2)=
| 0.64g |
| 64g/mol |
(4)根据反应的方程式Zn+2H2SO4=ZnSO4+SO2↑+2H2O、Zn+H2SO4=ZnSO4+H2↑计算,n(Zn)=n(SO2)+n(H2);
(5)若撤走盛有无水氯化钙的U型管,则氢氧化钠洗气瓶增重偏大;
(6)为了准确地测量气体体积,读数时应注意气体温度、压强等问题的影响.
解答:解:(1)检验气密性,可关闭分液漏斗活塞,向右侧球形管中加入水,一段时间后观察球形管和量气管之间的液面差有无变化,
故答案为:关闭分液漏斗活塞,向右侧球形管中加入水,一段时间后观察球形管和量气管之间的液面差有无变化;
(2)n(Zn)=0.02mol,理论生成n(H2)=0.02mol,v(H2)=0.02mol×22.4L/mol=0.448L=448mL,则应选择500mL量气管,故答案为:D;
(3)如发生Zn+2H2SO4=ZnSO4+SO2↑+2H2On(Zn)=0.02mol,应生成n(SO2)=
=0.01mol,小于0.02mol,说明还有氢气生成,还发生Zn+H2SO4=ZnSO4+H2↑,
故答案为:Zn+2H2SO4=ZnSO4+SO2↑+2H2O、Zn+H2SO4=ZnSO4+H2↑;
(4)反应的方程式Zn+2H2SO4=ZnSO4+SO2↑+2H2O、Zn+H2SO4=ZnSO4+H2↑,则n(Zn)=n(SO2)+n(H2),
所以
=
+
,
故答案为:
=
+
;
(5)若撤走盛有无水氯化钙的U型管,则氢氧化钠洗气瓶增重偏大,故答案为:偏小;
(6)为了准确地测量气体体积,读数时应注意气体温度、压强等问题的影响,则应注意①待冷却至室温再开始读数; ②读数前使量气管左右液面相平;③眼睛视线与液面最低处相平,
故答案为:①待冷却至室温再开始读数; ②读数前使量气管左右液面相平;③眼睛视线与液面最低处相平.
故答案为:关闭分液漏斗活塞,向右侧球形管中加入水,一段时间后观察球形管和量气管之间的液面差有无变化;
(2)n(Zn)=0.02mol,理论生成n(H2)=0.02mol,v(H2)=0.02mol×22.4L/mol=0.448L=448mL,则应选择500mL量气管,故答案为:D;
(3)如发生Zn+2H2SO4=ZnSO4+SO2↑+2H2On(Zn)=0.02mol,应生成n(SO2)=
| 0.64g |
| 64g/mol |
故答案为:Zn+2H2SO4=ZnSO4+SO2↑+2H2O、Zn+H2SO4=ZnSO4+H2↑;
(4)反应的方程式Zn+2H2SO4=ZnSO4+SO2↑+2H2O、Zn+H2SO4=ZnSO4+H2↑,则n(Zn)=n(SO2)+n(H2),
所以
| a |
| 65 |
| b |
| 64 |
| V |
| 22400 |
故答案为:
| a |
| 65 |
| b |
| 64 |
| V |
| 22400 |
(5)若撤走盛有无水氯化钙的U型管,则氢氧化钠洗气瓶增重偏大,故答案为:偏小;
(6)为了准确地测量气体体积,读数时应注意气体温度、压强等问题的影响,则应注意①待冷却至室温再开始读数; ②读数前使量气管左右液面相平;③眼睛视线与液面最低处相平,
故答案为:①待冷却至室温再开始读数; ②读数前使量气管左右液面相平;③眼睛视线与液面最低处相平.
点评:本题易浓硫酸的性质为载体综合考查化学实验设计,侧重于学生的分析能力和实验能力的考查,为高考常见题型,难度中等,注意把握实验原理.

练习册系列答案
 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案
相关题目
 不同浓度的硫酸与锌反应时,硫酸可以被还原为SO2,也可被还原为氢气.为了验证这一事实,某同学拟用如图装置进行实验(实验时压强为10lkPa,温度为0℃,锌的相对原子质量为65).
不同浓度的硫酸与锌反应时,硫酸可以被还原为SO2,也可被还原为氢气.为了验证这一事实,某同学拟用如图装置进行实验(实验时压强为10lkPa,温度为0℃,锌的相对原子质量为65).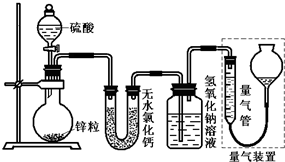 不同浓度的硫酸与锌反应时,硫酸可以被还原为SO2,也可被还原为氢气.为了验证这一事实,某同学拟用如图装置进行实验(实验时压强为10l kPa,温度为0℃).
不同浓度的硫酸与锌反应时,硫酸可以被还原为SO2,也可被还原为氢气.为了验证这一事实,某同学拟用如图装置进行实验(实验时压强为10l kPa,温度为0℃).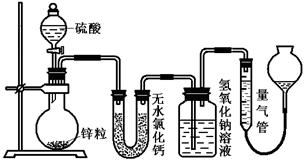
 应后锌有剩余,测得氢氧化钠洗气瓶增重mg,则整个实验过程产生的气体中,n(H2)/n(SO2)=_______________(用含字母的代数式表示)。若撤走盛有无水氯化钙的U型管,n(H2)/n(SO2)的数值将
应后锌有剩余,测得氢氧化钠洗气瓶增重mg,则整个实验过程产生的气体中,n(H2)/n(SO2)=_______________(用含字母的代数式表示)。若撤走盛有无水氯化钙的U型管,n(H2)/n(SO2)的数值将