题目内容
下列离子或分子在溶液中能大量共存,但通入NO2后不能大量共存,且不会生成沉淀的一组是( )
| A.K+、Na+、NO3-、SiO32- | B.Al3+、K+、SO42-、S2- |
| C.Ag+、Na+、NH3·H2O、NO3- | D.Cu2+、Fe2+、Cl-、SO42- |
D
解析试题分析:离子间如果发生化学反应,则不能大量共存,反之是可以的。A中离子可以大量共存,但通入NO2后,NO2与水反应生成硝酸,硝酸与SiO32-反应生成硅酸沉淀,不符合题意;B中Al3+与S2-不能大量共存,二者反应生成氢氧化铝沉淀和H2S气体,不符合题意;C中Ag+与NH3·H2O不能大量共存,二者反应可以生成白色沉淀氢氧化银,不符合题意;D中离子可以大量共存,但通入NO2后,NO2与水反应生成硝酸,硝酸具有强氧化性,能把Fe2+氧化生成铁离子,没有沉淀。符合题意,答案选D。
考点:考查离子共存的正误判断

练习册系列答案
 学业测评一课一测系列答案
学业测评一课一测系列答案 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案
相关题目
下列反应的离子方程式正确的是
A.NH4HCO3溶液与过量NaOH溶液共热:NH4++ OH一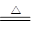 NH3↑+H2O NH3↑+H2O |
| B.Na2O2加入H218O中:2Na2O2+2H218O=4Na++4OH-+18O2↑ |
| C.向海带灰浸出液中加入稀硫酸、双氧水:2I-+2H++H2O2=I2+2H2O |
| D.Ba(OH)2溶液中滴加NaHSO4溶液至中性:Ba2++OH-+H++SO42一=BaSO4↓ +H2O |
能在水溶液中大量共存的一组离子是
| A.Na+、Mg2+、I-、ClO- | B.Al3+、NH4+、SO42-、Cl- |
| C.K+、Ag+、NO3-、Cl- | D.NH4+、Na+、OH-、SiO32- |
下列各组离子能大量共存的是
| A.NaClO水溶液中:Fe2+、Cl-、Ca2+、H+ |
| B.加入KSCN显红色的溶液:K+、Na+、I-、S2- |
| C.无色酸性溶液中:K+、CH3COO-、HCO3-、MnO4- |
| D.pH=2的溶液中:NH4+、Na+、Cl-、Cu2+ |
下列离子在溶液中能大量共存的一组是
| A.Fe3+、H+、ClO-、SO32- | B.K+、Al3+、Cl-、CO32- |
| C.Na+、Ca2+、HCO3-、OH- | D.Al3+、NH4+、Cl-、SO42- |
下列反应的离子方程式正确的是
A.将氯气溶于水制备次氯酸:Cl2+H2O 2H++Cl-+ClO- 2H++Cl-+ClO- |
| B.少量CO2通入苯酚钠溶液中:2C6H5O-+CO2+H2O=2C6H5OH+CO32- |
| C.Na2O2与H2O混合:2Na2O2+2H2O=4Na++4OH-+O2↑ |
D.向NH4HCO3溶液中加过量的NaOH溶液并加热:NH4++OH- NH3↑+H2O NH3↑+H2O |
下列离子方程式中,正确的
| A.在AlCl3溶液中加入过量氨水:Al3+ + 3NH3·H2O =Al(OH)3↓ + 3NH4+ |
| B.大理石加入过量盐酸中:CO32-+2H+= CO2↑+H2O |
| C.稀硫酸和Ba(OH)2溶液反应:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| D.在CuSO4溶液中加入Ba(OH)2溶液:Ba2+ + SO42- =BaSO4↓ |
下列离子方程式的书写正确的是( )
| A.铁和稀硫酸反应:2Fe + 6H+ =2Fe 3+ +3H 2↑ |
| B.NaHCO3溶液与NaOH溶液反应: OH― + HCO3―= CO32― + H2O |
| C.钠和冷水反应 Na+2H2O=Na++2OH-+H2↑ |
| D.氯化铝溶液中加入过量的氨水 Al3+ + 4NH3·H2O =AlO2- + 4NH4++ 2H2O |
(14分)氧化锌是橡胶、油漆、搪瓷、电缆、医药、电子、化学等工业的重要原料。以氧
化锌粗品为原料制备活性氧化锌的生产工艺流程如下: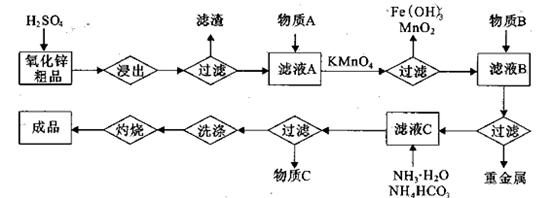
(1).浸出”后得到的酸性溶液中含有Zn2+、SO42-,另含有Fe2+、Cu2+、 +、Mn2+等
+、Mn2+等
杂质。物质A的作用是调节溶液的pH至5 4,物质A最好选择________。
| A.NH3.H2O | B.Na2CO3 | C.H2SO4 | D.ZnO |

该温度下
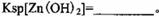 。
。(2) KMnO4的作用是除去Mn2+和Fe2+,则KMnO4与Mn2+反应的离子方程式为_____________________________________;若溶液中
 ,则处理1
,则处理1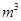 该溶液,Fe2+所消耗的KMnO4的质量为________g(保留两位有效数字)。
该溶液,Fe2+所消耗的KMnO4的质量为________g(保留两位有效数字)。(3)杂质Cu2+、
 2+可利用置换反应除去,则物质B是_________。
2+可利用置换反应除去,则物质B是_________。(4)被灼烧的沉淀是
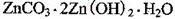 ,生成该沉淀的化学方程式为________。
,生成该沉淀的化学方程式为________。如何检验该沉淀是否洗净?________________________________。