题目内容
已知在一定条件下,CH4与NO2存在以下可逆反应:CH4(g)+4NO2(g) 4NO(g)+CO2(g)+2H2O(g);△H=-x
4NO(g)+CO2(g)+2H2O(g);△H=-x kJ/mol,现取12mol CH4与NO2的混合物在该条件下反应至平衡时,共转移电子16mol,并放出热量1148kJ,则该反应中的x值及12mol混合气体中CH4与NO2的物质的量之比为( )
A.x=1148,

B.x=574,

C.x=574,

D.x=574,

【答案】分析:反应中甲烷是还原剂,二氧化氮是氧化剂,甲烷中碳元素由-4价升高为+4价,根据电子转移可知,参加反应甲烷的物质的量为2mol,放出热量1148kJ,所以2x=1148,故x=574;
由于反应为可逆反应,所以混合气体中甲烷的物质的量大于2mol,由于有2mol的甲烷反应,所以二氧化氮的物质的量至少由8mol,据此判断合气体中CH4与NO2的物质的量之比.
解答:解:反应中甲烷是还原剂,二氧化氮是氧化剂,甲烷中碳元素由-4价升高为+4价,令参加反应的甲烷为ymol,根据电子转移可知,8y=16,解得y=2,所以参加反应甲烷的物质的量为2mol,放出热量1148kJ,所以2x=1148,故x=574;
由于反应为可逆反应,所以混合气体中甲烷的物质的量大于2mol,由于有2mol的甲烷反应,所以二氧化氮的物质的量至少由8mol,即甲烷的物质的量2mol<n(CH4)<12mol-8mol=4mol,8mol<n(NO2)<12mol-2mol=10mol.
所以混合气体中CH4与NO2的物质的量之比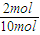 <
<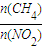 <
<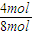 ,即
,即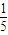 <
<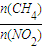 <
< .
.
故选:D.
点评:考查氧化还原反应的计算,难度中等,注意反应为可逆反应,根据可逆反应的特点判断甲烷与二氧化氮的范围是关键.
由于反应为可逆反应,所以混合气体中甲烷的物质的量大于2mol,由于有2mol的甲烷反应,所以二氧化氮的物质的量至少由8mol,据此判断合气体中CH4与NO2的物质的量之比.
解答:解:反应中甲烷是还原剂,二氧化氮是氧化剂,甲烷中碳元素由-4价升高为+4价,令参加反应的甲烷为ymol,根据电子转移可知,8y=16,解得y=2,所以参加反应甲烷的物质的量为2mol,放出热量1148kJ,所以2x=1148,故x=574;
由于反应为可逆反应,所以混合气体中甲烷的物质的量大于2mol,由于有2mol的甲烷反应,所以二氧化氮的物质的量至少由8mol,即甲烷的物质的量2mol<n(CH4)<12mol-8mol=4mol,8mol<n(NO2)<12mol-2mol=10mol.
所以混合气体中CH4与NO2的物质的量之比
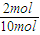 <
<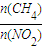 <
<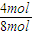 ,即
,即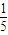 <
<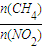 <
< .
.故选:D.
点评:考查氧化还原反应的计算,难度中等,注意反应为可逆反应,根据可逆反应的特点判断甲烷与二氧化氮的范围是关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 Ⅰ工业上常利用醋酸和乙醇合成有机溶剂乙酸乙酯:CH3COOH(l)+C2H5OH(l)
Ⅰ工业上常利用醋酸和乙醇合成有机溶剂乙酸乙酯:CH3COOH(l)+C2H5OH(l)| 浓H2SO4 |
| △ |
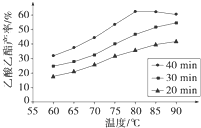
已知CH3COOH、C2H5OH和CH3COOC2H5的沸点依次为118℃、78℃和77℃.在其他条件相同时,某研究小组进行了多次实验,实验结果如图所示.(1)该研究小组的实验目的是
(2)60℃下反应40min与70℃下反应20min相比,前者的平均反应速率
(3)如图所示,反应时间为40min、温度超过80℃时,乙酸乙酯产率下降的原因可能是
Ⅱ.煤化工中常需研究不同温度下平衡常数、投料比及热值等问题.
已知:CO(g)+H2O(g)??H2(g)+CO2(g)平衡常数随温度的变化如下表:
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
(1)在800℃发生上述反应,以表中的物质的量投入恒容反应器,其中向正反应方向移动的有
| n(CO) | n(H2O) | n(H2) | n(CO2) | |
| A | 1 | 5 | 2 | 3 |
| B | 2 | 2 | 1 | 1 |
| C | 3 | 3 | 0 | 0 |
| D | 0.5 | 2 | 1 | 1 |
| E | 3 | 1 | 2 | 1 |
C(s)+H2O(g)??CO(g)+H2(g) 平衡常数为K1;
CO(g)+H2O(g)??H2(g)+CO2(g) 平衡常数为K2;
则K、K1、K2之间的关系是
(3)在V L密闭容器中通入10mol CO和10mol水蒸气,在T℃达到平衡,然后急速通过碱石灰,将所得混合气体燃烧,测得放出的热量为2 842kJ(已知CO燃烧热为283kJ?mol-1,H2燃烧热为286kJ?mol-1),则T℃平衡常数K=
 在一定条件下可以一步反应生成二元醇,例如:
在一定条件下可以一步反应生成二元醇,例如: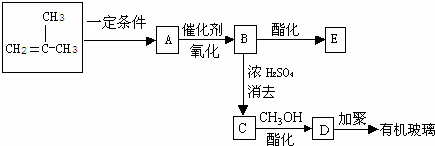
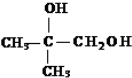

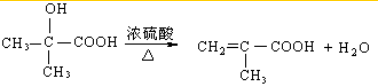



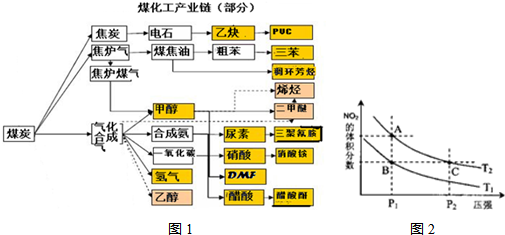
 和
和 .实验测得N-N键键能为167kJ?mol-1,NO2中氮氧键的键能为466kJ?mol-1,N2O4中氮氧键的键能为438.5kJ?mol-1.请写出NO2转化为N2O4的热化学方程式
.实验测得N-N键键能为167kJ?mol-1,NO2中氮氧键的键能为466kJ?mol-1,N2O4中氮氧键的键能为438.5kJ?mol-1.请写出NO2转化为N2O4的热化学方程式 H2(g)+CO2(g)的平衡常数随温度的变化如表:
H2(g)+CO2(g)的平衡常数随温度的变化如表: 2CO(g)平衡常数K;
2CO(g)平衡常数K; CO(g)+H2(g) 平衡常数K1;
CO(g)+H2(g) 平衡常数K1; H2(g)+CO2(g) 平衡常数K2,
H2(g)+CO2(g) 平衡常数K2,