��Ŀ����
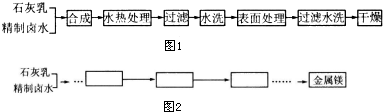
7��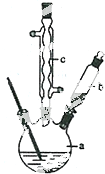 ������ͭ�Ǻϳ��������������в���--��������ͭ����Ҫǰ����֮һ������������һ��ʵ���Һϳ�·�ߣ�
������ͭ�Ǻϳ��������������в���--��������ͭ����Ҫǰ����֮һ������������һ��ʵ���Һϳ�·�ߣ�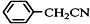 +H2O+H2SO4$\stackrel{100-130��}{��}$
+H2O+H2SO4$\stackrel{100-130��}{��}$ +NH4HSO4
+NH4HSO4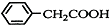 +Cu��OH��2��
+Cu��OH��2��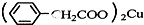 +H2O
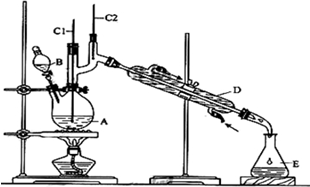
+H2O�Ʊ��������װ��ʾ��ͼ��ͼ�����Ⱥͼг�װ�õ��ԣ�����֪����������۵�Ϊ76.5�棬������ˮ�������Ҵ����ش��������⣺
��1����250mL����ƿa�м���70mL70%���ᣮ���ƴ�����ʱ����������ˮ��Ũ������Ⱥ�˳�����ȼ�ˮ���ټ���Ũ���ᣮ
��2����a�е���Һ������100�棬�����μ�40g�����浽������Һ�У�Ȼ��������130�������Ӧ����װ���У�����b�������ǵμӱ����棻����c�����������������ܣ��������ǻ�������ʹ��������������������Ӧ�������������ˮ���ٷ�����������Ʒ��������ˮ��Ŀ���DZ��ڱ��������������������п����ڷ��뱽�����Ʒ����BCE�����ţ�
A����Һ©�� B��©�� C���ձ� D��ֱ��������E��������
��3���ᴿ�ֱ�����ķ������ؽᾧ�����յõ�44g��Ʒ��������IJ�����95%��
��4����CuCl2•2H2O��NaOH��Һ�Ʊ�����Cu��OH��2�����������������ˮϴ�ӳ������жϳ���ϴ�ɾ���ʵ�������������ȡ���һ������ϴ��Һ������ϡ���ᣬ�ټ���AgNO3��Һ���ް�ɫ���dz��֣�
��5������������˵��Ҵ���ˮ�Ļ���ܼ��У�����ܽ����Cu��OH��2����30min�����ˣ���Һ����һ��ʱ�䣬����������ͭ���壬����ܼ����Ҵ����������������ܽ�ȣ����ڳ�ַ�Ӧ��
���� ��1�����ƴ�����ʱ��Ӧ���ܶȴ��ע���ܶ�С��Һ���У���ֹ���ʱ�ų���ʹҺ�ηɽ���
��2����ͼ��֪��cΪ�����ܣ�ʹ������Һ����������������b�ɼ��뷴ӦҺ����Ӧ�������������ˮ�������¶ȣ���С��������ܽ�ȣ����뱽�����Ʒ�����ù��˲�����
��3��������������ˮ����ˮ�е��ܽ�Ƚ�С���ɷ�Ӧ +H2O+H2SO4 $\stackrel{100��130��}{��}$
+H2O+H2SO4 $\stackrel{100��130��}{��}$ +NH4HSO4��֪��40g���������ɱ�����Ϊ40g��$\frac{136}{117}$=46.5g��
+NH4HSO4��֪��40g���������ɱ�����Ϊ40g��$\frac{136}{117}$=46.5g��
��4��������ˮϴ�ӳ�������������ϴ�Ӹɾ�����������������ϴ��Һȷ���Ƿ�ϴ�Ӹɾ���
��5��������������ˮ�������Ҵ�������ܼ����Ҵ�������������ܽ�ȣ�
��� �⣺��1��ϡ��Ũ����ų��������ȣ����ƴ�����ʱ��Ӧ���ܶȴ��ע���ܶ�С��Һ���У���ֹ���ʱ�ų���ʹҺ�ηɽ������������ˮ��Ũ������Ⱥ�˳�����ȼ�ˮ���ټ���Ũ���ᣬ
�ʴ�Ϊ���ȼ�ˮ���ټ���Ũ���
��2����ͼ��֪��cΪ���������ܣ�������Ϊ��������ʹ�����ķ�ӦҺ������������b������Ϊ�μӱ����棻��Ӧ�������������ˮ�������¶ȣ���С��������ܽ�ȣ��������ˮ�ɱ��ڱ��������������뱽�����Ʒ�����ù��˲���������Ҫ������Ϊ©�����ձ�����������
�ʴ�Ϊ���μӱ����棻���������ܣ���������ʹ�����ķ�ӦҺ�����������ڱ�����������BCE��
��3��������������ˮ����ˮ�е��ܽ�Ƚ�С�����ᴿ������ķ������ؽᾧ���ɷ�Ӧ +H2O+H2SO4 $\stackrel{100��130��}{��}$
+H2O+H2SO4 $\stackrel{100��130��}{��}$ +NH4HSO4��֪��40g���������ɱ�����Ϊ40g��$\frac{136}{117}$=46.5g�����յõ�44g��Ʒ��������IJ�����$\frac{44g}{46.5g}$��100%=95%��
+NH4HSO4��֪��40g���������ɱ�����Ϊ40g��$\frac{136}{117}$=46.5g�����յõ�44g��Ʒ��������IJ�����$\frac{44g}{46.5g}$��100%=95%��
�ʴ�Ϊ���ؽᾧ��95%��
��4��������ˮϴ�ӳ�������������ϴ�Ӹɾ�����������������ϴ��Һȷ���Ƿ�ϴ�Ӹɾ��������ϴ�ɾ���ʵ�������������ȡ���һ������ϴ��Һ������ϡ���ᣬ�ټ���AgNO3��Һ���ް�ɫ���dz��֣�
�ʴ�Ϊ��ȡ���һ������ϴ��Һ������ϡ���ᣬ�ټ���AgNO3��Һ���ް�ɫ���dz��֣�
��5��������������ˮ�������Ҵ�������ܼ����Ҵ�������������ܽ�ȣ�Ȼ����Cu��OH��2��Ӧ��ȥ�����ᣬ������ܼ����Ҵ������������������ܽ�ȣ����ڳ�ַ�Ӧ��
�ʴ�Ϊ�����������ܽ�ȣ����ڳ�ַ�Ӧ��
���� ���⿼�鱽����ͭ�ĺϳɣ����������Ʊ�ʵ�鼰�л������ʵĿ��飬���պϳɷ�Ӧ��ʵ��װ�õ�����Ϊ���Ĺؼ����ۺϿ���ѧ��ʵ�鼼�ܺͷ�������������������Ŀ�Ѷ��еȣ�ע����Ϣ�Ĵ�����Ӧ�ã�

 ����ʦ���һ��һ��ϵ�д�
����ʦ���һ��һ��ϵ�д� �Ͻ�ƽ��У����ϵ�д�
�Ͻ�ƽ��У����ϵ�д�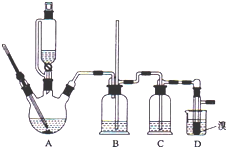 ʵ�����Ʊ� 1��2-��������ķ�Ӧԭ�����£�
ʵ�����Ʊ� 1��2-��������ķ�Ӧԭ�����£�CH3CH2OH��CH2=CH2+H2OC H2=CH2+Br2��BrCH2CH2Br
���ܴ��ڵ���Ҫ����Ӧ�У��Ҵ���Ũ����Ĵ������� l40����ˮ�������ѣ�������������������Ҵ��Ʊ�1��2-���������װ����ͼ��ʾ���й��������б����£�
| �Ҵ� | 1��2-�������� | ���� | |
| ״̬ | ��ɫҺ�� | ��ɫҺ�� | ��ɫҺ�� |
| �ܶ�/g•cm-3 | 0.79 | 2.2 | 0.71 |
| �е�/�� | 78.5 | 132 | 34.6 |
| �۵�/�� | -130 | 9 | -116 |
��1���ڴ��Ʊ�ʵ���У�Ҫ������Ѹ�ٵذѷ�Ӧ�¶���ߵ� 170�����ң�������ҪĿ����d��������ȷѡ ��ǰ����ĸ��
a��������Ӧb���ӿ췴Ӧ�ٶ�c����ֹ�Ҵ��ӷ�d�����ٸ�������������
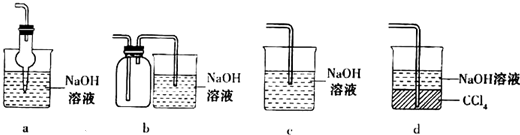
��2����װ�� C ��Ӧ����NaOH��Һ����Ŀ�������շ�Ӧ�п������ɵ��������� ������ȷѡ��ǰ����ĸ�� a��ˮb��Ũ����c������������Һd������̼��������Һ
��3���жϸ��Ʊ���Ӧ�Ѿ�������������������ɫ��ȫ��ȥ��
��4���� 1��2-��������ֲ�Ʒ���ڷ�Һ©���м�ˮ�����ã�����Ӧ���²㣨��ϡ������¡�����
��5����������������δ��Ӧ�� Br2�������bϴ�ӳ�ȥ������ȷѡ��ǰ����ĸ����
a��ˮb������������Һc���⻯����Һd���Ҵ�
��6�������������������������ѣ����õķ�����ȥ����
��7����Ӧ������Ӧ����ˮ��ȴװ�� D������ҪĿ������ȴ�ɱ�����Ĵ����ӷ������ֲ��ܹ�����ȴ�����ñ�ˮ������ԭ����1��2-������������̵�ϵͣ�9�棩��������ȴ��ʹ�����̶�ʹ��·������

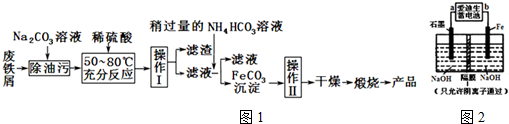
��֪Cu2+��Fe3+��Fe2+���������↑ʼ�����ͳ�����ȫʱ��pH��������
| Fe3+ | Fe2+ | Cu2+ | |
| �������↑ʼ����ʱ��PH | 1.9 | 7.0 | 4.7 |
| ����������ȫ����ʱ��PH | 3.2 | 9.0 | 6.7 |
��1�����ʺ���������X����C��
A��K2Cr207 B��NaCl0 C��H202 D��KMn04
��2�����������Y��AC��
A��CuO B��NaOH����������C��Cu2��OH��2CO3����D��NH3
��3������Һ����CuCl2•2H2O����Ҫ��������Ũ������ȴ�ᾧ�����˲�����
��4���ⶨ��Һ����Fe2+��Ũ�ȣ�����KMnO4����Һ�ζ���ȡ��KMnO4��ҺӦʹ����ʽ������ʽ����ʽ�����ζ��ܣ���Ӧ�Ļ�ѧ����ʽ��MnO4-+8H++5Fe2+=Mn2++5Fe3++4H2O��
�����ķ�Ӧ���£�
CH3CH2CH2CH2OH$��_{H_{2}SO_{4}��}^{Na_{2}Cr_{2}O_{2}}$CH3CH2CH2CHO
��Ӧ��Ͳ��������������£�
| �е�/�� | �ܶȣ�g��cm-3�� | ˮ���ܽ��� | |
| ������ | 117.2 | 0.8109 | �� |
| ����ȩ | 75.5 | 0.8107 | �� |
�ٽ�6.0gNa2Cr2O7����100mL�ձ��У���30mLˮ�ܽ⣬�ٻ�������5mLŨ���ᣬ��������ҺС��ת����B�У�
����A�м���4.0g�������ͼ�����ʯ�����ȣ�������������ʱ����ʼ�μ�B����Һ���μӹ����б��ַ�Ӧ�¶�Ϊ90��95�棬��E���ռ�90�����µ���֣�
�۽�����ﵹ���Һ©���У���ȥˮ�㣬�л������������ռ�75��77����֣�����2.0g��
�ش��������⣺
��1��B�����������Ƿ�Һ©����D������������ֱ�������ܣ�
��2����ʯ�������Ƿ�ֹ���У�
��3��������ȩ�ֲ�Ʒ���ڷ�Һ©���з�Һʱ��ˮ���²㣨��ϡ����¡���
��4����Ӧ�¶�Ӧ������90��95�棬��ԭ���DZ�֤����ȩ��ʱ�������ֿɾ��������䱻��һ��������
��5����ʵ���У�����ȩ�IJ���Ϊ51%��