题目内容
下列各图中表示化学方程式A(g)+B(g)?C(g)+D(g)△H<0的是(E表示能量,n表示物质的量)( )
分析:分析反应是气体体积不变的放热反应,反应物能量高于生成物,依据能量高低、化学平衡移动原理分析判断选项.
解答:解:A、图象中反应物能量低于生成物,反应是吸热反应,故A不符合;
B、图象中反应物能量高于生成物,符合反应进程,故B符合;
C、反应过程中拆化学键需要吸收能量,图象中能量变化不符合,故C不符合;
D、反应是放热反应,温度升高平衡逆向进行,A物质的量增大,与图象不符,故D不符合;
故选B.
B、图象中反应物能量高于生成物,符合反应进程,故B符合;
C、反应过程中拆化学键需要吸收能量,图象中能量变化不符合,故C不符合;
D、反应是放热反应,温度升高平衡逆向进行,A物质的量增大,与图象不符,故D不符合;
故选B.
点评:本题考查了反应能量变化的分析判断,注意反应过程分析,平衡移动原理的应用,题目较简单.

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
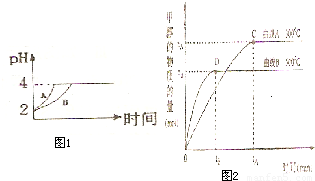
 化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题:
化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题: 化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题:
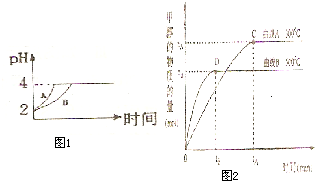
化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题: 4C (g) △H >0 达到平衡时,c(A) ="2" mol·L-1,c ( B) =" 7" mol·L-1,c ( C) =" 4" mol·L-1。试确定B的起始浓度c (B)的取值范围是 ;若改变条件重新达到平衡后体系中C的质量分数增大,下列措施可行的是 。
4C (g) △H >0 达到平衡时,c(A) ="2" mol·L-1,c ( B) =" 7" mol·L-1,c ( C) =" 4" mol·L-1。试确定B的起始浓度c (B)的取值范围是 ;若改变条件重新达到平衡后体系中C的质量分数增大,下列措施可行的是 。
 4C (g) △H >0 达到平衡时,c(A) ="2" mol·L-1,c ( B) =" 7" mol·L-1,c ( C) =" 4" mol·L-1。试确定B的起始浓度c (B)的取值范围是 ;若改变条件重新达到平衡后体系中C的质量分数增大,下列措施可行的是 。
4C (g) △H >0 达到平衡时,c(A) ="2" mol·L-1,c ( B) =" 7" mol·L-1,c ( C) =" 4" mol·L-1。试确定B的起始浓度c (B)的取值范围是 ;若改变条件重新达到平衡后体系中C的质量分数增大,下列措施可行的是 。