题目内容
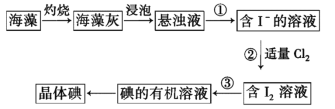
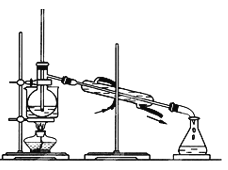
【题目】叠氮化钠(NaN3)是一种无色无味的晶体,他在医药、炸药、照相药剂、树脂及农药合成等中应用广泛,它又是汽车安全气囊最理想的气体发生原料。有关他的制取以及纯度测定实验如下,试分析并回答:
(1)①方法一,液氨法,液氨与金属钠反应生成NaNH2,再与笑气反应(NaNH2+N2O→NaN3+NaOH+Y),Y的常用检测检验方法是_____________;
②方法二,水合肼法,N2H4H2O+NaOH+C2H5ONO= NaN3+C2H5O H+3H2O,C2H5ONO即亚硝酸乙酯,可用乙醇、硫酸与NaNO2来制取,其中C2H5ONO从组成看,可用另一种同分异构体代替:___________(写名称);由此有人提出用N2H4与NaNO2在一定条件下直接制取NaN3,其化学方程式是__________;
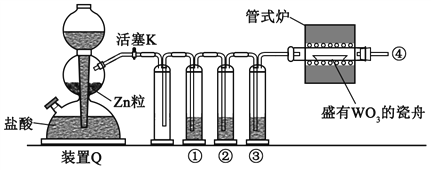
③方法三,尿素法,尿素[CO(NH2)2]与硝酸、浓硫酸、锌电解还原、NaNO2及脱水等经一系列反应后生成NH2CON3,后者再与NaOH反应,即发生NH2CON3+NaOH→NaN3+Y+Z+H2O,生成NaN3,则Z的俗名是_____。
(2)采用如下装置测定NaN3纯度:准确称量1.40克NaN3样品,与NaClO反应产生N2并放出热量(注:杂质不与NaClO反应)。
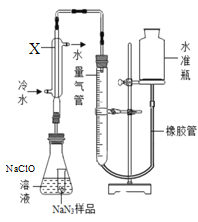
①使小试管中的NaN3样品与NaClO溶液接触的操作是____________;该反应的化学方程式是___________;
②仪器X的名称是____________,使用冷水冷凝的目的是冷却生成的气体及____;反应前应将液面调节到量气筒的“0”刻度,并使两边液面相平,反应后读数时,还需要进行的操作是__________;
③常温下量气筒读数为672mL(N2的密度为1.25 gL-1)。则该NaN3样品的纯度是_______。
【答案】用湿润的红色石蕊试纸检验,试纸变蓝色 硝基乙烷 ![]() 纯碱或苏打 将锥形瓶倾斜
纯碱或苏打 将锥形瓶倾斜 ![]() (直形)冷凝管 除去生成的气体中的水蒸气 调节量气管,使两侧的液面保持水平 约92.9%
(直形)冷凝管 除去生成的气体中的水蒸气 调节量气管,使两侧的液面保持水平 约92.9%
【解析】
(1)①根据元素守恒,反应前后原子的种类与数目保持不变判断气体为氨气,结合氨气的检验方法回答;
②分子式相同,结构不同的有机物互为同分异构体;根据酯类水解反应与已知反应利用盖斯定律的理论分析化学方程式;
③依据元素守恒规律判断化学方程式;
(2)①根据仪器的使用方法分析;结合氧化还原反应的规律书写离子方程式;
②根据仪器的构造与用途回答;反应可能产生水蒸气,使用冷水冷凝可除去生成的气体中的水蒸气;量气管读数前,需要平衡压强;
③先根据体积和密谋计算氮气的体积,再利用关系式2NaN3→3N2计算NaN3样品的纯度。
(1)①NaNH2与N2O反应可生成NaN3、NaOH和NH3,则Y为NH3,用湿润的红色石蕊试纸检验,若试纸变蓝色,则该气体为NH3,故答案为:用湿润的红色石蕊试纸检验,试纸变蓝色;
②C2H5ONO与硝基乙烷互为同分异构体,可用硝基乙烷来代替;亚硝酸乙酯在碱性条件下可发送水解生成乙醇与亚硝酸钠,因此N2H4H2O+NaOH+C2H5ONO= NaN3+C2H5OH+3H2O可用N2H4与NaNO2在一定条件下直接制取NaN3,变换后的化学方程式为:![]() ,故答案为:硝基乙烷;
,故答案为:硝基乙烷;![]() ;
;
③NH2CON3+NaOH→NaN3+Y+Z+H2O,Y为NH3,生成的Z为Na2CO3,其俗名为纯碱或苏打;
(2)①根据图示装置可知,将锥形瓶倾斜可使小试管中的NaN3样品与NaClO溶液接触,NaClO具有氧化性,可将NaN3转化为N2,自身被还原为NaCl,则反应的化学方程式为:![]() ,故答案为:将锥形瓶倾斜;
,故答案为:将锥形瓶倾斜;![]() ;
;
②图示X为(直形)冷凝管;反应可能产生水蒸气,使用冷水冷凝的还可除去生成的气体中的水蒸气;量气管读数前,需要调节量气管使两侧的液面保持水平,确保气体压强与外界大气压强相等,故答案为:(直形)冷凝管;除去生成的气体中的水蒸气;调节量气管,使两侧的液面保持水平;
③生成氮气的质量为![]() =0.84g,
=0.84g,
设NaN3样品的纯度X,
2NaN3 ![]() 2Na+3N2↑
2Na+3N2↑
130 84
x1.40g 0.084g
![]() 解得:x
解得:x![]() 92.9%,故答案为:约92.9%。
92.9%,故答案为:约92.9%。

 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案