题目内容
(1)氨气在工农业有着广泛的用途。已知25%氨水的密度为0.91 g/cm3,5%氨水的密度为0.98 g/cm3。
①配制100mL 2.5mol/L氨水需要浓度为25%氨水______mL(保留2位小数)。
②若将上述两溶液等体积混合,所得氨水溶液的质量分数是_____________。
A.等于15% B.大于15% C.小于15% D.无法估算
已知:4NH3+O2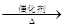 4NO+6 H2O,4NO+3O2+2H2O
4NO+6 H2O,4NO+3O2+2H2O 4HNO3
4HNO3
(2)设空气中氧气的体积分数为0.20,氮气的体积分数为0.80。
①a mol NO完全转化为HNO3理论上需要氧气_____________mol。
②为使NH3恰好完全氧化为NO,氨-空气混合气体中氨的体积分数(用小数表示)为_____________
(保留2位小数)。
(3)20.0 mol NH3用空气氧化,产生混合物的组成为:NO 18.0 mol、O2 12.0 mol、N2 150.0 mol和一定量硝酸,以及其他成分(高温下NO与O2不化合)。计算氨转化为NO和HNO3的转化率。
(4)20.0 mol NH3和一定量空气充分反应后,再转化为硝酸。通过计算,在图中画出HNO3的物质的量n(A)和空气的物质的量n (B)关系的理论曲线。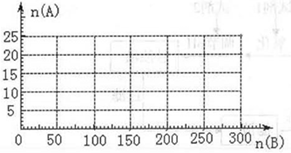
①配制100mL 2.5mol/L氨水需要浓度为25%氨水______mL(保留2位小数)。
②若将上述两溶液等体积混合,所得氨水溶液的质量分数是_____________。
A.等于15% B.大于15% C.小于15% D.无法估算
已知:4NH3+O2
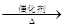 4NO+6 H2O,4NO+3O2+2H2O
4NO+6 H2O,4NO+3O2+2H2O 4HNO3
4HNO3(2)设空气中氧气的体积分数为0.20,氮气的体积分数为0.80。
①a mol NO完全转化为HNO3理论上需要氧气_____________mol。
②为使NH3恰好完全氧化为NO,氨-空气混合气体中氨的体积分数(用小数表示)为_____________
(保留2位小数)。
(3)20.0 mol NH3用空气氧化,产生混合物的组成为:NO 18.0 mol、O2 12.0 mol、N2 150.0 mol和一定量硝酸,以及其他成分(高温下NO与O2不化合)。计算氨转化为NO和HNO3的转化率。
(4)20.0 mol NH3和一定量空气充分反应后,再转化为硝酸。通过计算,在图中画出HNO3的物质的量n(A)和空气的物质的量n (B)关系的理论曲线。

(本题共16分)(1)①18.68mL ②C
(2)①0.75a ②0.14
(3)7.5%;97.5%
(4)
(2)①0.75a ②0.14
(3)7.5%;97.5%
(4)

试题分析:(1)①根据c=
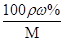 可知,浓氨水的物质的量浓度c=
可知,浓氨水的物质的量浓度c=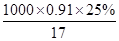 mol/L=13.4mol/L。设浓氨水的体积为V,则2.5mol/L×0.1L=13.4mol/L×V,解得V=0.01868L=18.68mL。
mol/L=13.4mol/L。设浓氨水的体积为V,则2.5mol/L×0.1L=13.4mol/L×V,解得V=0.01868L=18.68mL。②若两种氨水等质量混合,则混合后氨水的质量分数等于15%。等体积的两种氨水,浓度大的氨水的密度较小,所以质量较小,两种氨水混合后,质量分数更接近稀氨水的浓度,因此所得氨水溶液的质量分数小于15%,因此答案选C。
(2)①根据化学反应方程式4NO+3O2+2H2O→4HNO3可知,a mol NO完全转化为HNO3理论上需要氧气=
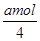 ×3=0.75amol。
×3=0.75amol。②假设氨气的体积是4L,设需要空气的体积为y,则根据化学反应方程式可知
4NH3 + 5O2
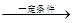 4NO+6H2O
4NO+6H2O4L 5L
4L 0.20y
解得y=
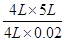 =25L
=25L所以氨-空气混合物中氨的体积分数=
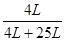 =0.14
=0.14(3)设生成x mol HNO3,根据反应式4NH3+5O2
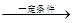 4NO+6 H2O、4NO+3O2+2H2O→4HNO3可知NH3+2O2→HNO3+H2O,由于空气中氮气的量是氧气的4倍,所以4(2x+18.0×
4NO+6 H2O、4NO+3O2+2H2O→4HNO3可知NH3+2O2→HNO3+H2O,由于空气中氮气的量是氧气的4倍,所以4(2x+18.0×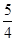 +12.0)=150.0,解得x=1.5mol。根据氮原子守恒,NH3的转化为HNO3的转化率=
+12.0)=150.0,解得x=1.5mol。根据氮原子守恒,NH3的转化为HNO3的转化率=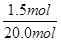 ×100%=7.5%;NH3的转化为NO的转化率=
×100%=7.5%;NH3的转化为NO的转化率=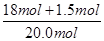 ×100%=97.5%。
×100%=97.5%。(4)根据反应4NH3+5O2
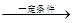 4NO+6 H2O①和4NO+3O2 +2H2O→4HNO3②可知,将(①+②)÷2得到反应NH3+2O2→H2O+HNO3③。由①③知,当n(O2):n(NH3)≤5:4,即n(空气):n(NH3)≤25:4时无硝酸生成,此时20.0mol氨气所需空气量为
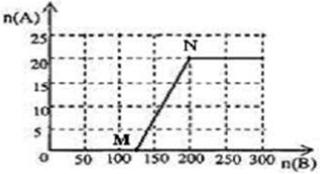
4NO+6 H2O①和4NO+3O2 +2H2O→4HNO3②可知,将(①+②)÷2得到反应NH3+2O2→H2O+HNO3③。由①③知,当n(O2):n(NH3)≤5:4,即n(空气):n(NH3)≤25:4时无硝酸生成,此时20.0mol氨气所需空气量为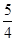 ×20.0mol×5=125mol;当5:4≤n(O2):n(NH3)≤2:1,即25:4≤n(空气):n(NH3)≤10:1时有硝酸生成,此时20.0mol氨气所需空气量为5×2××20.0mol=200mol,生成硝酸的物质的量是20mol,所以HNO3的物质的量n(A)和空气的物质的量n (B)关系的理论曲线为
×20.0mol×5=125mol;当5:4≤n(O2):n(NH3)≤2:1,即25:4≤n(空气):n(NH3)≤10:1时有硝酸生成,此时20.0mol氨气所需空气量为5×2××20.0mol=200mol,生成硝酸的物质的量是20mol,所以HNO3的物质的量n(A)和空气的物质的量n (B)关系的理论曲线为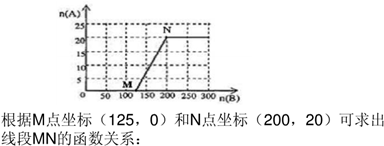 。
。
练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 g
g







