题目内容
amolFe与一定量的硝酸在一定条件下充分反应,将生成的气体与标准状况下b g O2混合,恰好能被水完全吸收,则a和b的关系可能是
| A.0.5a≤b≤0.75a | B.16a≤b≤24a | C.0.2a≤b≤0.3a | D.无法确定 |
B
试题分析:amolFe与一定量的硝酸在一定条件下充分反应,将生成的气体与标准状况下b g O2混合,恰好能被水完全吸收,则根据电子得失守恒可知,铁失去的电子恰好被氧气得到。如果铁失去2个电子,则2a=
 ×4,解得b=16a;如果铁失去3个电子,则3a=
×4,解得b=16a;如果铁失去3个电子,则3a= ×4,解得b=24a,所以a和b的关系可能是16a≤b≤24a,答案选B。
×4,解得b=24a,所以a和b的关系可能是16a≤b≤24a,答案选B。
练习册系列答案
 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案
相关题目
 ×100%
×100%  mol·L-1
mol·L-1 mol·L-1+c(H+)
mol·L-1+c(H+) 
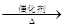 4NO+6 H2O,4NO+3O2+2H2O
4NO+6 H2O,4NO+3O2+2H2O 4HNO3
4HNO3