��Ŀ����
I. һ�������£������Ϊ3 L���ܱ������У�һ����̼��������Ӧ���ɼ״�������ΪCu2O/ZnO����CO��g����2H2��g��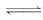 CH3OH��g����
CH3OH��g����
�������������ͼ��������и��⣺��Ӧ�ﵽƽ��ʱ��ƽ�ⳣ������ʽK�� ��
��2�������¶ȣ�Kֵ ���������С�����䡱����
II. ���淴Ӧ��aA��g��+ bB��g��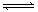 cC��g��+ dD��g��������ͼ�ش�
cC��g��+ dD��g��������ͼ�ش�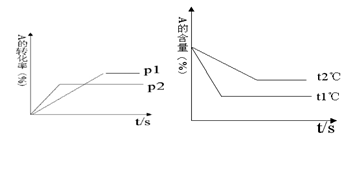
��1��ѹǿ P1��P2 ������С������2����a +b���ȣ�c +d�� ������С����
��3���¶�t1���t2�� �����ͣ�����4������ӦΪ ��Ӧ��
I��1��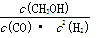 ����2����С II��1��С��2��С ��3���ߣ�4������
����2����С II��1��С��2��С ��3���ߣ�4������
�������������I.��1����ѧƽ�ⳣ������һ�������£������淴Ӧ�ﵽƽ��״̬ʱ��������Ũ�ȵ���֮���ͷ�Ӧ��Ũ�ȵ���֮���ı�ֵ�����Ը��ݷ���ʽ��֪ƽ�ⳣ������ʽK��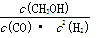 ��
��
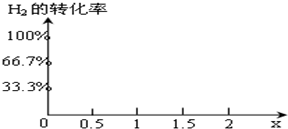
��2������ͼ���֪���¶�Խ�ߣ��״������ʵ���Խ�٣���˵�������¶�ƽ�����淴Ӧ�����ƶ������������¶�ƽ�ⳣ����С��
II��1��ѹǿΪP2ʱ���ȴﵽƽ��״̬������ѹǿ P1��P2С��
��2��ѹǿ�ߣ���Ӧ���ת���ʵͣ���˵������ѹǿƽ�����淴Ӧ�����ƶ�����������Ӧ���������Ŀ��淴Ӧ����a +b���ȣ�c +d��С��
��3���¶�Ϊt1ʱ���ȴﵽƽ��״̬�����¶�t1���t2��ߡ�
��4���¶ȸ߷�Ӧ���ת���ʵͣ���˵�������¶�ƽ�����淴Ӧ�����ƶ�����������Ӧ�Ƿ��ȷ�Ӧ��
���㣺���鷴Ӧ���ʡ�ƽ�ⳣ�����йؼ����Լ����������ƽ��״̬��Ӱ��
�������������е��Ѷȵ����⣬���������ǿ�����ض�ѧ������֪ʶ�Ĺ��̺�ѵ��������Ĺؼ�����ȷ��Ӧ���ʺ�ƽ�ⳣ���ĺ����Լ�Ӱ�����أ�Ȼ������ͼ��ͷ���ʽ���������������ԭ���жϼ��ɡ�����������ѧ�������������������ѧ�����������ɡ��ܽ������������

 Сѧ��10���ӿ������100��ϵ�д�
Сѧ��10���ӿ������100��ϵ�д� CH3OCH3��g��+3H2O��g������H��0��
CH3OCH3��g��+3H2O��g������H��0��
 CH3OH��g����
CH3OH��g����
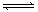 cC��g��+ dD��g��������ͼ�ش�
cC��g��+ dD��g��������ͼ�ش�