题目内容
【题目】关于水溶液中的离子平衡,下列说法正确的是
A.往![]() 稀溶液中加入NaOH固体,溶液中
稀溶液中加入NaOH固体,溶液中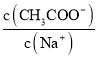 变大
变大
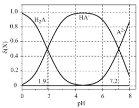
B.等物质的量浓度的![]() 、
、![]() 、
、![]() 三种溶液中,
三种溶液中,![]() 的大小顺序为:
的大小顺序为:![]()
C.常温下![]() 的
的![]() 溶液和
溶液和![]() 的NaOH溶液等体积混合,溶液中离子浓度大小顺序为:
的NaOH溶液等体积混合,溶液中离子浓度大小顺序为:![]()
D.![]() 的
的![]() 溶液中:
溶液中:![]()
【答案】C
【解析】
A.加入NaOH固体,会导致钠离子浓度增大,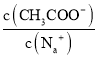 会变小,A错误;
会变小,A错误;
B.物质的量浓度相等的![]() 、
、![]() 、
、![]() 三种溶液中,
三种溶液中,![]() 中
中![]() 促进了
促进了![]() 的水解,
的水解,![]() 中铝离子水解抑制了铵根离子的水解,则
中铝离子水解抑制了铵根离子的水解,则![]() 中NH4+浓度大于
中NH4+浓度大于![]() ,所以
,所以![]() 由大到小的顺序为:
由大到小的顺序为:![]() ,B错误;
,B错误;
C.醋酸是弱酸,在溶液中存在电离平衡,所以在常温下pH=2 CH3COOH溶液中c(CH3COOH)>0.01mol/L,pH=2 的CH3COOH和![]() 的NaOH溶液等体积混合,CH3COOH过量,溶液为CH3COOH和CH3COONa的混合溶液,CH3COOH电离作用大于CH3COO-的水解作用,溶液显酸性,所以溶液中离子浓度大小顺序为:
的NaOH溶液等体积混合,CH3COOH过量,溶液为CH3COOH和CH3COONa的混合溶液,CH3COOH电离作用大于CH3COO-的水解作用,溶液显酸性,所以溶液中离子浓度大小顺序为:![]() ,C正确;
,C正确;
D.![]() 的
的![]() 溶液中,根据物料守恒,
溶液中,根据物料守恒,![]() ,D错误;
,D错误;
故合理选项是C。

 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案【题目】由已知电离常数判断,下列关于SO2与Na2CO3(aq)反应的离子方程式的书写中,不合理的是( )
酸 | 电离常数 |
碳酸 | K1=4×10-7 K2=5.6×10-11 |
亚硫酸 | K1=1.54×10-2 K2=1.02×10-7 |
A.SO2+H2O+2CO32-=2HCO3-+SO32-
B.SO2+H2O+CO32-=H2O+CO2+SO32-
C.2SO2+2H2O+CO32-=H2O+CO2+2HSO3-
D.SO2+H2O+CO32-=HCO3-+HSO3-
【题目】氨气是一种重要化工原料。
(1)德国化学家哈伯从1902年开始研究由氮气和氢气直接合成氨。
已知:①![]() △H=a kJ/mol
△H=a kJ/mol
②每破坏lmol有关化学键需要的能量如下表:
H-H | N-H | N≡N |
436kJ | 391kJ | 946k |
则a=_________________。
(2)下图为不同温度(T)、不同投料比[n(![]() )/n(
)/n(![]() )]时反应达到平衡时
)]时反应达到平衡时![]() 的转化率变化曲线。
的转化率变化曲线。

①![]() 、
、![]() 、
、![]() 、
、![]() 的大小关系为__________________。
的大小关系为__________________。
②保持温度和体积不变,提高投料比[n(![]() )/n(
)/n(![]() )],则重新达到平衡时,下列说法一定正确的是_______(填字母序号)。
)],则重新达到平衡时,下列说法一定正确的是_______(填字母序号)。
A.![]() 的浓度增大
的浓度增大
B.![]() 的转化率增大
的转化率增大
C.![]() 的体积分数增大
的体积分数增大
D.![]() 的浓度减小
的浓度减小
③温度为![]() 时,向2L密闭容器中加入1.0mol
时,向2L密闭容器中加入1.0mol![]() 和1.0mol
和1.0mol![]() ,若5min后反应达到平衡,则用v(
,若5min后反应达到平衡,则用v(![]() )表示该反应的平均速率为____________________;反应在
)表示该反应的平均速率为____________________;反应在![]() 时的平衡常数K=________________。
时的平衡常数K=________________。
(3)一种新型除烟气中氮氧化物的方法是采用![]() 作还原剂还原烟气中的氮氧化物且产物无污染,写出
作还原剂还原烟气中的氮氧化物且产物无污染,写出![]() 还原
还原![]() 的化学反应方程式_____________________________________。
的化学反应方程式_____________________________________。
(4)若用标准盐酸测定某稀氨水的浓度,应选择__________作指示剂;滴定过程中眼睛注视_____________。已知稀氨水体积为25.0mL,滴定结束测得消耗0.0100mol/L盐酸的平均体积为20.0mL,则该氨水的浓度为________________(保留2位有效数字);若滴定前滴定管尖嘴有气泡,滴定后尖嘴无气泡,则测定结果________(填“偏大”、“偏小”、“不变”)。