题目内容
【题目】我们利用物质的结构与性质对周期表进行研究,有助于我们更好地掌握同类知识。
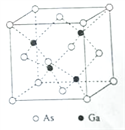
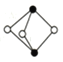
(1)基态砷原子中,价电子占用_________个原子轨道;雌黄分子式为As2S3,分子结构如图,则As原子的杂化方式为_________ 。
(2)N2与CO互为等电子体,则1molCO分子中含有的π键数目是_________个。
(3)向CuSO4溶液中加人少量氨水生成蓝色沉淀,继续加人过量氨水沉淀溶解,得到深蓝色透明溶液,最后向该溶液中加人一定量乙醇,析出[Cu(NH3)4]SO4 .H2O晶体;该晶体所含的非金厲元素中,N、O、S第一电离能由大到小的顺序是_________ (填元素符号),SO42-的空间构型为____________,晶体中含有的化学键有__________。加人乙醇后析出[Cu(NH3)4]SO4 .H2O晶体的原因是____________。
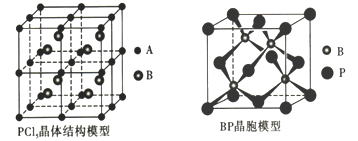
(4)常温下PCl5是一种白色晶体,其立方晶系晶体结构模型如下左图所示,由A、B两种微粒构成。 将其加热至148℃熔化,形成一种能导电的熔体。已知A微粒与CCl4具有相同的空间构型和相似的化学键特征,则A为_________ , B为_______________。
(5)磷化硼(BP)是一种超硬耐磨涂层材料,下右图为其立方晶胞。已知晶体中最近的硼原子和磷原子核间距为x cm,磷化硼的摩尔质量为bg.·mol-1,阿伏加德罗常数为NA,则磷化硼晶体密度的表达式
为____________g.cm-3。(列出计算式即可)
【答案】 4 sp3杂化 2NA(或2×6.02×1023) N>O>S 正四面体 离子键、极性共价键和配位键 乙醇分子极性比水分子极性弱,加入乙醇降低溶剂的极性,从而减小溶质的溶解度 PCl4+ PCl6- ![]()
【解析】(1)基态砷原子中,价电子排布式为4s24p3,根据洪特规则,4p轨道的3个电子要分占不同的轨道并且自旋状态相同,所以其价电子共占用4个原子轨道;由雌黄分子结构示意图可知,每个As原子与3个S原子形成3个σ键,由于其价电子数是5个,所以该分子中砷原子有1个孤电子对,根据价层电子对互斥理论,中心原子的价电子对数为4,所以中心原子的杂化方式为sp3杂化。
(2)N2与CO互为等电子体,氮气分子中有叁键,叁键中有1个σ键、2个π键,等电子体之间结构相似,所以CO分子中也有2个π键,则1molCO分子中含有的π键数目是2NA(或2×6.02×1023)个。
(3) 一般非金属性越强的元素的第一电离能也越大,但是每个周期的IIA(s轨道全满)和VA(p轨道半充满)元素因其原子结构的特殊性,其第一电离能高于相邻元素,所以N、O、S第一电离能由大到小的顺序是N>O>S。SO42-的中心原子价电子对数n=![]() =4,中心原子形成了4个σ键,所以其空间构型为正四面体。[Cu(NH3)4]SO4H2O晶体是一种配合物,其内界中中心原子铜离子和配体氨分子之间形成配位键,氨分子内有极性键,外界硫酸根与内界之间形成离子键。加人乙醇后析出[Cu(NH3)4]SO4H2O晶体的原因是乙醇分子极性比水分子极性弱,加入乙醇降低溶剂的极性,从而减小溶质的溶解度。
=4,中心原子形成了4个σ键,所以其空间构型为正四面体。[Cu(NH3)4]SO4H2O晶体是一种配合物,其内界中中心原子铜离子和配体氨分子之间形成配位键,氨分子内有极性键,外界硫酸根与内界之间形成离子键。加人乙醇后析出[Cu(NH3)4]SO4H2O晶体的原因是乙醇分子极性比水分子极性弱,加入乙醇降低溶剂的极性,从而减小溶质的溶解度。
(4) A微粒与CCl4具有相同的空间构型和相似的化学键特征,所以A与四氯化碳是等电子体,则A为PCl4+ ,由质量守恒和电荷守恒可知 B为PCl6- 。
(5)该晶胞中含有4个B原子和4个P原子。如果把晶胞分成8个相同的小立方,则B原子恰好可以位于其中4个小立方的体心,设晶胞的边长为2a,晶体中最近的硼原子和磷原子核间距为x cm,则xcm= ![]() ,所以a=
,所以a= ![]() ,1mol该晶胞的体积为
,1mol该晶胞的体积为![]() =
=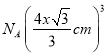 ,磷化硼的摩尔质量为bg.·mol-1,则1mol该晶胞中含BP 4mol,其质量为4bg,所以磷化硼晶体密度的表达式 为
,磷化硼的摩尔质量为bg.·mol-1,则1mol该晶胞中含BP 4mol,其质量为4bg,所以磷化硼晶体密度的表达式 为![]() g.cm-3。
g.cm-3。