题目内容
用蒸馏水逐渐稀释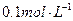 的醋酸,若维持温度不变,则在稀释过程中逐渐增大的是( )
的醋酸,若维持温度不变,则在稀释过程中逐渐增大的是( )
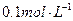 的醋酸,若维持温度不变,则在稀释过程中逐渐增大的是( )
的醋酸,若维持温度不变,则在稀释过程中逐渐增大的是( )A.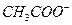 的物质的量浓度 的物质的量浓度 | B.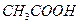 的物质的量浓度 的物质的量浓度 |
| C.H+的物质的量浓度 | D.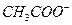 和H+的物质的量 和H+的物质的量 |
D
略

练习册系列答案
相关题目
题目内容
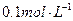 的醋酸,若维持温度不变,则在稀释过程中逐渐增大的是( )
的醋酸,若维持温度不变,则在稀释过程中逐渐增大的是( )A.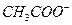 的物质的量浓度 的物质的量浓度 | B.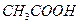 的物质的量浓度 的物质的量浓度 |
| C.H+的物质的量浓度 | D.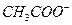 和H+的物质的量 和H+的物质的量 |
