题目内容
弱电解质的电离程度可用电离度(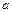 )表示:
)表示: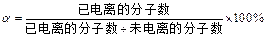 ,现有pH均为4的HCl和
,现有pH均为4的HCl和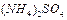 溶液,则两种溶液中H2O的电离度之比为( )
溶液,则两种溶液中H2O的电离度之比为( )
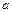 )表示:
)表示: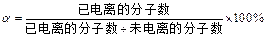 ,现有pH均为4的HCl和
,现有pH均为4的HCl和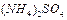 溶液,则两种溶液中H2O的电离度之比为( )
溶液,则两种溶液中H2O的电离度之比为( )| A.1:2 | B.2:5 | C.1:106 | D.106:1 |
C
略

练习册系列答案
相关题目
题目内容
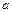 )表示:
)表示: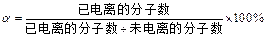 ,现有pH均为4的HCl和
,现有pH均为4的HCl和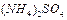 溶液,则两种溶液中H2O的电离度之比为( )
溶液,则两种溶液中H2O的电离度之比为( )| A.1:2 | B.2:5 | C.1:106 | D.106:1 |
