题目内容
18.2003年10月15日我国成功发射了第一艘载人航天飞船-“神州五号”.从此我国进入了航天大国和航天强国行列.发射“神五”用肼(N2H4)作为火箭发动机的燃料,NO2为氧化剂,反应生成N2和水蒸气.已知:N2(g)+2O2(g)=2NO2(g);△H=+67.7kJ/mol.
N2H4(g)+O2(g)=N2(g)+2H2O(g);△H=-534kJ/mol.
下列关于肼和NO2反应的热化学方程式中,正确的是( )
| A. | 2N2H4(g)+2NO2(g)=3N2(g)+4H2O(l);△H=-1135.7 kJ/mol | |
| B. | 2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g);△H=-1000.3 kJ/mol | |
| C. | N2H4(g)+NO2(g)=3/2N2(g)+2H2O(l);△H=-1135.7 kJ/mol | |
| D. | 2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g);△H=-1135.7 kJ/mol |
分析 已知:N2(g)+2O2(g)=2NO2(g);△H=+67.7kJ/mol ①
N2H4(g)+O2(g)=N2(g)+2H2O(g);△H=-534kJ/mol ②
根据肼和NO2反应的化学方程式为2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g)可知:将②×2-①可得,反应热做相应的变化即可.
解答 解:已知:N2(g)+2O2(g)=2NO2(g);△H=+67.7kJ/mol ①
N2H4(g)+O2(g)=N2(g)+2H2O(g);△H=-534kJ/mol ②
根据肼和NO2反应的化学方程式为2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g)可知:将②×2-①可得2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g)△H=(-534kJ/mol )×2-(+67.7kJ/mol )=-1135.7KJ/mol,故选D.
点评 本题考查了盖斯定律的应用,根据所给的反应做相应的变形来构建目标反应,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.2015年8月12日天津港危险品仓库发生的爆炸事故,再次警示人们在注重提高科技化工发展水平的同时,不可忽视化学试剂存放的基本问题.下列在实验室中关于试剂存放叙述正确的是( )

| A. | 白磷不易挥发,不需要密闭存放 | |
| B. | 氢氧化钠溶液应保存在带玻璃塞的细口试剂瓶中 | |
| C. | 氰化物的包装标签上应贴上如图所示的标志 | |
| D. | 用容量瓶配制好溶液进行贮存时,需在容量瓶上贴上浓度标签 |
9.下列除去杂质的方法,正确的是( )
| A. | 苯中含有苯酚杂质:加入溴水,过滤 | |
| B. | 乙醇中含有乙酸杂质:加入碳酸钠溶液,分液 | |
| C. | CuCl2溶液中含有FeCl3杂质:加入过量氧化铜粉末,过滤 | |
| D. | CO2中含有HCl杂质:通入饱和Na2CO3溶液,洗气 |
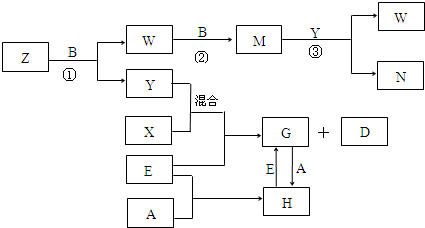
6.反应中 ,W为( )
,W为( )
 ,W为( )
,W为( )| A. | CH3CHO | B. | CH3CH2OH | C. | CH3COOH | D. | H2O |
13.NA表示阿伏加德罗常数,下列说法中正确的是( )
| A. | 常温常压下,7.1gCl2含有的Cl2分子数为0.2NA | |
| B. | 0.1 mol羟基(-OH)含有的电子数为NA | |
| C. | 1.7gNH3含有的电子数为NA | |
| D. | 标准状况下,11.2LSO3中含有的氧原子数为1.5NA |
3.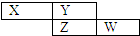 X、Y、Z、W均为短周期元素,它们在周期表的位置如图所示,若W原子的最外层电子数是内层电子总数的$\frac{7}{10}$,下列说法中正确的是( )
X、Y、Z、W均为短周期元素,它们在周期表的位置如图所示,若W原子的最外层电子数是内层电子总数的$\frac{7}{10}$,下列说法中正确的是( )
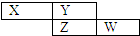 X、Y、Z、W均为短周期元素,它们在周期表的位置如图所示,若W原子的最外层电子数是内层电子总数的$\frac{7}{10}$,下列说法中正确的是( )
X、Y、Z、W均为短周期元素,它们在周期表的位置如图所示,若W原子的最外层电子数是内层电子总数的$\frac{7}{10}$,下列说法中正确的是( )| A. | 阴离子的半径从大到小排列顺序为:X>Y>Z>W | |
| B. | X元素的氢化物分子间可以形成氢键 | |
| C. | Y的两种同素异形体在常温下可以相互转化 | |
| D. | 最高价氧化物对应的水化物的酸性:W>Z |
10.下列关于铜电极的叙述中不正确的是( )
| A. | 铜锌原电池中铜是正极 | |
| B. | 用电解法电解氯化钠溶液时,铜可作阴极 | |
| C. | 用电解法精炼粗铜时粗铜作阴极 | |
| D. | 在镀件上电镀铜时可用金属铜作阳极 |