题目内容
【题目】已知反应 Fe(s) + CO2(g) ![]() FeO(s) + CO(g),△H=aKJ﹒mol-1,平衡常数为K。测得在不同温度下,K值如下:
FeO(s) + CO(g),△H=aKJ﹒mol-1,平衡常数为K。测得在不同温度下,K值如下:
温度/℃ | 500 | 700 | 900 |
K | 1.00 | 1.47 | 2.4 |
(1)若500℃时进行反应①,CO2的起始浓度为2mol﹒L-1,CO的平衡浓度为__________。
(2)该反应为__________(选填“吸热”或“放热”)反应。
(3)700℃时反应达到平衡,要使该平衡向右移动,其他条件不变时,可以采取的措施有__________(填序号)。
A.缩小反应器体积 B.CO2 C.升高温度到900℃ D.使用合适的催化剂
E.增加Fe的量
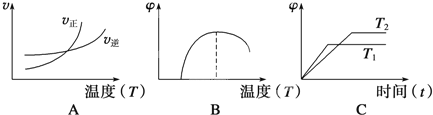
(4)下列图像符合该反应的是__________(填序号)(图中v为速率,φ为混合物中CO含量,T为温度且T1>T2)。
【答案】
(1)1mol·L-1;(2)吸热;(3)BC;(4)A
【解析】
试题分析:(1)令平衡时CO的浓度为cmol/L,则:
Fe(s)+CO2(g)![]() FeO(s)+CO(g)
FeO(s)+CO(g)
开始(mol/L): 2 0
变化(mol/L): c c
平衡(mol/L): 2-c c
则:![]() =1,解得:c=1,故答案为:1mol/L;
=1,解得:c=1,故答案为:1mol/L;
(2)由表中数据可知,升高温度,平衡常数增大,反应向正反应方向移动,则正反应为吸热反应,即a>0,故答案为:吸热;
(3)A.反应是前后气体体积不变的反应,缩小反应器体积,体系的压强增大,但平衡不移动,故A错误;B.通入CO2,增大反应物浓度平衡向正反应方向移动,故B正确;C.图表数据可知,升高温度到900℃,平衡常数增大,平衡向正反应方向移动,故C正确;D.使用合适的催化剂,只能加快反应速率,同等程度增大正逆反应速率,平衡不移动,故D错误;E、固体对平衡无影响,增加Fe的量对平衡无影响,故E错误;故答案为:BC;
(4)A、由图可知,升高温度,平衡向正反应移动,故图象表示正反应吸热反应,反应①正反应是吸热反应,图象与实际相符合,故A正确;B、由图可知,最高点到达平衡,温度升高,混合物中CO的含量降低,平衡向逆反应进行,故图象表示正反应为放热反应,反应①正反应是吸热反应,图象与实际不相符,故B错误;C、由图可知,温度T1先到达平衡,故温度T1>T2,温度T1到达平衡时,混合物中CO的含量降低,平衡向逆反应进行,故图象表示正反应为放热反应,反应①正反应是吸热反应,图象与实际不相符,故C错误;故答案为:A。

 阅读快车系列答案
阅读快车系列答案
