题目内容
【题目】50mL0.50mol·L-1盐酸与50mL0.55mol·L-1NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
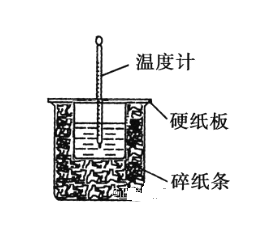
(1)从实验装置上看,图中尚缺少的一种玻璃仪器有___。
(2)烧杯间填满碎纸条的作用是___。
(3)大烧杯上如不盖硬纸板,求得的中和热数值___(填“偏大”“偏小”“无影响”)。
(4)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热的数值会___;用50mL浓硫酸代替盐酸溶液进行上述实验,测得的中和热的数值会___。(均填“偏大”“偏小”“无影响”)
【答案】环形玻璃搅拌棒 减小实验过程中的热量损失 偏小 偏小 偏大
【解析】
(1)、根据量热计的构造来判断该装置缺少的仪器;
(2)、中和热测定实验成败的关键是保温工作;
(3)、大烧杯上如不盖硬纸板,会使一部分热量散失;
(4)、根据弱电解质电离吸热分析。
(1)、由量热计的构造可知该装置的缺少仪器是环形玻璃搅拌棒,
故答案为:环形玻璃搅拌棒;
(2)、中和热测定实验成败的关键是保温工作,大小烧杯之间填满碎泡沫塑料的作用是减少实验过程中的热量损失,
故答案为:减少实验过程中的热量损失;
(3)、大烧杯上如不盖硬纸板,会使一部分热量散失,求得的中和热数值将会减小,
故答案为:偏小;
(4)、氨水为弱碱,电离过程为吸热过程,所以用氨水代替稀氢氧化钠溶液反应,反应放出的热量偏小,求得的中和热数值将会减小,若用50mL浓硫酸代替盐酸溶液进行上述实验,浓硫酸溶于水会放出大量的热,反应放出的热量偏大,测得的中和热的数值会偏大,
故答案为:偏小;偏大。

 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案 高效智能课时作业系列答案
高效智能课时作业系列答案【题目】根据下列事实得出的结论正确的是( )。
选项 | 事实 | 结论 |
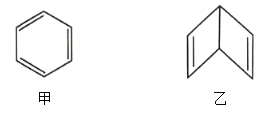
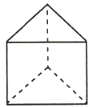
A | 甲、乙两种有机物具有相同的相对分子质量和不同的结构 | 甲和乙一定互为同分异构体 |
B | 质量相同的甲、乙两种有机物完全燃烧时产生质量相同的水 | 甲、乙两种分子中, |
C | 在淀粉溶液中加入稀硫酸,水浴加热一段时间后取出部分水解液,滴加银氨溶液后再加热,无银镜出现 | 淀粉的水解产物不具有还原性 |
D | 不存在两种邻二甲苯 | 苯分子中的碳碳键完全相同,苯不是单双键交替结构 |
A.AB.BC.CD.D