题目内容
【题目】下列说法中错误的是( )
A.SO2、SO3都是极性分子
B.在![]() 和[Cu(NH3)4]2+中都存在配位键
和[Cu(NH3)4]2+中都存在配位键
C.元素电负性越大的原子,吸引电子的能力越强
D.金刚石晶体中碳原子以共价键结合,具有键能大、熔点高、硬度大的特性
【答案】A
【解析】
本题利用一些常见的分子和离子综合考查了极性分子和非极性分子、配位键、电负性、晶体结构及其性质等相关知识。
A. SO3是平面三角形结构,属于非极性分子,SO2是V型结构,是极性分子,A错误;
B. ![]() 中氮原子提供孤电子对给氢离子,[Cu(NH3)4]2+中氮原子提供孤电子对给铜离子,都存在配位键,B正确;
中氮原子提供孤电子对给氢离子,[Cu(NH3)4]2+中氮原子提供孤电子对给铜离子,都存在配位键,B正确;
C. 电负性是元素的原子在化合物中吸引电子的能力的标度,元素的电负性越大,表示其原子在化合物中吸引电子的能力越强,C正确;
D. 金刚石是原子晶体,晶体中碳原子以共价键结合,共价键键能大,使得金刚石熔点高、硬度大,D正确。
答案选A。

【题目】碱式碳酸铜[Cu(OH)2CuCO3]是一种用途广泛的化工产品,实验室制备碱式碳酸铜的反应原理为:2CuSO4+2Na2CO3+H2O=Cu(OH)2CuCO3↓+CO2↑+2Na2SO4。回答下列问题:
(1)配制100mL浓度均为0.50molL-1的CuSO4溶液和Na2CO3溶液,需要用到的玻璃仪器有量筒、烧杯、胶头滴管和___。
(2)取50mL0.50molL-1CuSO4溶液加入50mL0.50molL-1Na2CO3溶液中,反应后烧杯底部出现大量蓝绿色沉淀。设计实验证明蓝绿色沉淀中混有难溶于水的碱式硫酸铜[Cu2(OH)2SO4],实验步骤是:过滤,___。
(3)按最佳配比 n(CuSO4)︰n(Na2CO3)=1︰1.2进行实验,反应15min,所得实验结果如下:
温度/℃ | 60 | 65 | 75 | 80 | 90 |
沉淀量/g | 1.295 | 1.303 | 1.451 | 1.340 | 1.292 |
分析75℃时沉淀量最多的原因:___。
(4)查阅资料可知碱式碳酸铜的组成有多种,可用xCu(OH)2yCuCO3表示。某小组利用以下装置测定某碱式碳酸铜样品的组成:
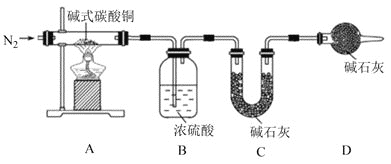
①A中发生反应的化学方程式是___。
②加热时持续通入N2的目的是___。
③称取32.0g样品,充分反应后得到24.0g残留物,B增重3.6g,C增重4.4g。该样品的化学式为___。若对调B和C装置的位置,___(填“能”或“不能”)测算出该样品的化学式。