��Ŀ����
����Ŀ���¶�Ϊ![]() ʱ���������ݻ���Ϊ
ʱ���������ݻ���Ϊ![]() �ĺ����ܱ������н�������Ӧ��
�ĺ����ܱ������н�������Ӧ��![]() ����Ӧ����
����Ӧ����![]() ��ʵ���ã�
��ʵ���ã�![]() ��
��![]() ��
��![]() ��
��![]() Ϊ���ʳ��������¶�Ӱ�졣ƽ�ⳣ��
Ϊ���ʳ��������¶�Ӱ�졣ƽ�ⳣ��![]() ����ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ
����ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ![]() ��ѹ
��ѹ![]() ���ʵ�������������˵������ȷ����
���ʵ�������������˵������ȷ����![]()
![]()
���� ��� | ���ʵ���ʼŨ�� | ���ʵ�ƽ��Ũ�� | ||
|
|
|
| |
�� |
| 0 | 0 |
|
�� |
|
|
| |
�� | 0 |
|
| |
A.��ƽ��ʱ����������![]() ���������е�С
���������е�С
B.������Ӧ��ƽ��ǰ��![]()
C.��ʼʱ����������ѹǿΪ![]() ����
����![]() ʱ�÷�Ӧ��ƽ�ⳣ��
ʱ�÷�Ӧ��ƽ�ⳣ��![]() kPa
kPa
D.���¶ȸı�Ϊ![]() ʱ����
ʱ����![]() ��
��![]()
���𰸡�D
��������
A.I�еķ�Ӧ![]()
![]()
��ʼ![]() 0 0
0 0
��Ӧ![]()
![]()
![]()
ƽ��![]()
![]()
![]()
��ѧƽ�ⳣ��![]() ���������ƽ��ʱ
���������ƽ��ʱ![]() ����μӷ�Ӧ��
����μӷ�Ӧ��![]() ����
����![]() ��
��![]() ��ƽ��ʱ
��ƽ��ʱ![]() ��
��![]() ������
������ ��˵��II��ƽ��ʱӦ�ô���
��˵��II��ƽ��ʱӦ�ô���![]() ������I��
������I��![]() �����Դ�ƽ��ʱ����������
�����Դ�ƽ��ʱ����������![]() С��1����������
С��1����������![]() ���������е�С����A��ȷ��
���������е�С����A��ȷ��
B. ����Aѡ����ƽ�ⳣ��K=1��![]() ����Ӧ����������У�����
����Ӧ����������У�����![]() ����B��ȷ��
����B��ȷ��
C. I�еķ�Ӧ![]()
![]()
��ʼ![]() 0 0
0 0
��Ӧ![]()
![]()
![]()
ƽ��![]()
![]()
![]()
ƽ��ʱ��ѹǿΪ![]() ����
����![]() ʱ�÷�Ӧ��ƽ�ⳣ��
ʱ�÷�Ӧ��ƽ�ⳣ��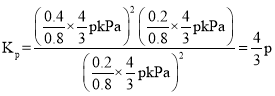 kPa��C��ȷ��
kPa��C��ȷ��
D.![]() ��
��![]() ���ﵽƽ��״̬ʱ���淴Ӧ������ȣ���
���ﵽƽ��״̬ʱ���淴Ӧ������ȣ���![]() ����
����![]() ����
����![]() ����ѧƽ�ⳣ��K����1�����¶��µ�K����
����ѧƽ�ⳣ��K����1�����¶��µ�K����![]() ���Ҹ÷�Ӧ������Ӧ�����ȷ�Ӧ�������¶�ƽ�������ƶ���K��������
���Ҹ÷�Ӧ������Ӧ�����ȷ�Ӧ�������¶�ƽ�������ƶ���K��������![]() ����D����
����D����
��ѡD��

����Ŀ��![]() ��Ϊһ����Ҫ����ԭ�ϣ�������Ӧ���ڹ�ҵ�����������й����ʷ�Ӧ�Ĵ����о������������863�ƻ���
��Ϊһ����Ҫ����ԭ�ϣ�������Ӧ���ڹ�ҵ�����������й����ʷ�Ӧ�Ĵ����о������������863�ƻ���
(1)���������н�ǿ��ѡ���ԣ���רһ�ԡ���֪��
��ӦI��![]()
��ӦII��![]()
д��NO�ֽ�����![]() ��
��![]() ���Ȼ�ѧ����ʽ______��
���Ȼ�ѧ����ʽ______��
(2)�ں��º���װ���г���һ������![]() ��
��![]() ����ij�����������½��з�ӦI����ò�ͬʱ���
����ij�����������½��з�ӦI����ò�ͬʱ���![]() ��
��![]() ����Ũ�������
����Ũ�������
ʱ�� | 0 | 5 | 10 | 15 | 20 | 25 |
|
|
|
|
|
|
|
|
|
|
|
|
|
�������й���������ȷ����______��
A.ʹ�ô���ʱ���ɽ��÷�Ӧ�Ļ�ܣ��ӿ��䷴Ӧ����
B.�����������![]() ʱ��˵����Ӧ�Ѵ�ƽ��
ʱ��˵����Ӧ�Ѵ�ƽ��
C.��������![]() ʱ��˵����Ӧ�Ѵ�ƽ��
ʱ��˵����Ӧ�Ѵ�ƽ��
D.ǰ10�����ڵ�ƽ������![]()
![]()
(3)��������ʱ�ᷢ����������������ӦI��![]() Ϊ����ij�����Ը÷�Ӧ��ѡ���ԣ���1L�ܱ������г���1mol
Ϊ����ij�����Ը÷�Ӧ��ѡ���ԣ���1L�ܱ������г���1mol![]() ��2mol
��2mol![]() ������й����ʵ�����ϵ��ͼ1��
������й����ʵ�����ϵ��ͼ1��

�ٸô����ڵ���ʱѡ��Ӧ______![]() ����I������II��
����I������II��![]() ��
��
��![]() ʱ��
ʱ��![]() ��ƽ�ⳣ��
��ƽ�ⳣ��![]() ______
______![]() ��Ҫ��ó���������ֻ���г����ּ���ʽ
��Ҫ��ó���������ֻ���г����ּ���ʽ![]() ��
��
��![]() ���B����������NO�����ʵ����ٵ���Ҫԭ��______��
���B����������NO�����ʵ����ٵ���Ҫԭ��______��
(4)�ϳɰ���ҵ���������������![]() ����ҵ�ϳ��ø�Ũ�ȵ�
����ҵ�ϳ��ø�Ũ�ȵ�![]() ��Һ����
��Һ����![]() ������ҺX�������õ�ⷨʹ
������ҺX�������õ�ⷨʹ![]() ��Һ��������װ����ͼ2��ʾ��
��Һ��������װ����ͼ2��ʾ��
���������������ķ�Ӧ����______��![]() ��
��
�ڼ���![]() ��������������ԭ��______��
��������������ԭ��______��
(5)�Ʊ�����ʱ������һ���ķ�Һ����ҵ�ϳ�������������ͳ�ȥ��Һ�е�![]() ��
��
��֪��![]() ʱ��
ʱ��![]() ��
��![]() ��
��![]()
���ڼ�����Һ�е�����Ũ��ʱ���漰����ĵ���ͨ��Ҫ���н��ƴ�������![]() �������
�������![]() ______
______![]() ȡ��������
ȡ��������![]() ��
��
����֪��ij��Һ�ӽ������ԣ������������������ᣬ����Һ��![]() ______
______![]() ������������λ��Ч����
������������λ��Ч����![]() ���ͻ����CuS������
���ͻ����CuS������
����Ŀ���ϳɰ���ҵ�漰����ȼ�ϵ���������Ҫ�о�CO2��CO֮���ת����Ϊ��Ū������ɣ���һ������CO2������̼������ɱ���ܱ������з�Ӧ��C(s)��CO2(g) ![]() 2CO(g) H�����ѹǿ���¶ȶ�CO��CO2��ƽ����ɵ�Ӱ����ͼ��ʾ���ش��������⣺
2CO(g) H�����ѹǿ���¶ȶ�CO��CO2��ƽ����ɵ�Ӱ����ͼ��ʾ���ش��������⣺

��1��p1��p2��p3�Ĵ�С��ϵ��________��ͼ��a��b��c�����Ӧ��ƽ�ⳣ����С��ϵ��______________________��
��2��һ�������£���CO2������̼��Ӧ����ƽ����ϵ�м���H2���ʵ������������з�Ӧ��������Ӧ1��CO(g)��3H2(g) ![]() CH4(g)��H2O(g) H1= a kJ/mol
CH4(g)��H2O(g) H1= a kJ/mol
��Ӧ2��CO(g)��H2O(g) ![]() CO2(g)��H2(g) H2= b kJ/mol
CO2(g)��H2(g) H2= b kJ/mol
�� �������̼��������Ӧת��Ϊ�����ˮ�������Ȼ�ѧ����ʽ��____________��
�� ��֪298 Kʱ��ػ�ѧ����������Ϊ��
��ѧ�� | H��H | O��H | C��H |
|
E/��kJ��mol-1�� | 436 | 465 | 413 | 1076 |
����ݼ��ܼ��㣬H1=________________����Ӧ1�Է����е�������___________���������ϸ��¶��������ϵ��¶������������¶�����
��3��һ�������£�CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) ��H3����̶��ݻ�Ϊ1 L���ܱ������г���2 mol CO2��6 mol H2��һ��ʱ���ﵽƽ��״̬�����CH3OH(g)�����ʵ���Ϊ1mol����������¸÷�Ӧ�Ļ�ѧƽ�ⳣ��K =_________���÷�����ʾ��������ʼʱ����2 mol CH3OH(g) ��2 mol H2O(g)�ﵽ��ͬƽ��״̬ʱ��CH3OH��ת����Ϊ_______����ƽ����ٳ���4 mol��N2����c(CO2)��ԭƽ��Ƚ���_________��������������������С��������������
CH3OH(g)+H2O(g) ��H3����̶��ݻ�Ϊ1 L���ܱ������г���2 mol CO2��6 mol H2��һ��ʱ���ﵽƽ��״̬�����CH3OH(g)�����ʵ���Ϊ1mol����������¸÷�Ӧ�Ļ�ѧƽ�ⳣ��K =_________���÷�����ʾ��������ʼʱ����2 mol CH3OH(g) ��2 mol H2O(g)�ﵽ��ͬƽ��״̬ʱ��CH3OH��ת����Ϊ_______����ƽ����ٳ���4 mol��N2����c(CO2)��ԭƽ��Ƚ���_________��������������������С��������������
��4����ͼ�Ǽ״�ȼ�ϵ�ع�����ʾ��ͼ������A��B��D��Ϊʯī�缫��CΪͭ�缫������һ��ʱ��Ͽ�K����ʱA��B�����ϲ��������������ͬ��

�����и����ĵ缫��ʽΪ_______________������C���ĵ缫��ӦʽΪ___________��
�� ����A�������������ڱ�״���µ����Ϊ__________________��
����Ŀ��ijѧ����0.10 mol��L��1��NaOH��Һ�ζ�ijŨ�ȵ����ᡣ��¼�������£�
ʵ�� ��� | ����Һ ���/mL | ������NaOH��Һ�����/mL | |
�ζ�ǰ����/mL | �ζ������/mL | ||
1 | 20.00 | 0.50 | 20.54 |
2 | 20.00 | 6.00 | 26.00 |
3 | 20.00 | 1.40 | 21.36 |

��1���ζ�ʱѡ�÷�̪��Һ��ָʾ��������жϵζ��ﵽ�յ�____________��
��2���ζ������У��۾�Ӧע��_____________________��
��3����������ʵ���Ũ��Ϊ___________��
��4����ʽ�ζ��ܼ��첿�������ݣ��ζ�����ʧ���Բⶨ�����Ӱ����__________(����ƫ������ƫ����������Ӱ����)��
��5��ijͬѧ����֪ȷŨ�ȵĸ��������Һ�ζ���Һ��Fe2����Ũ�ȣ����������ҺӦʢ����________(����������������)�У��÷�Ӧ�����ӷ���ʽΪ_______________

