题目内容
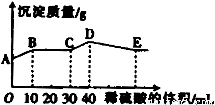
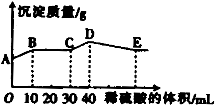
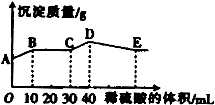
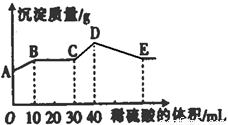
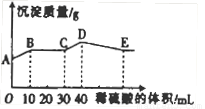
将由NaOH、BaCl2、Al2(SO4)3三种固体组成的混合物溶于足量的水中,充分溶解,向混合物液中滴加1mol?L-1的稀硫酸,加入稀硫酸的体积与生成沉淀的质量关系如图所示.下列有关判断不正确的是( )

| A.AB段发生反应的离子方程式为:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O |
| B.BC段发生反应的离子方程式为:H++OH-=H2O |
| C.D点表示的沉淀的化学式为Al(OH)3、BaSO4 |
| D.E点表示的溶液呈中性 |
由A点可知,A点白色硫酸钡沉淀,则BaCl2过量,由NaOH、BaCl2、Al2(SO4)3三种固体组成的混合物溶于足量的水中,充分溶解,混合液中含有钡离子、氢氧根离子、偏铝酸根离子、硫酸根离子,
A.由图象可知,AB段发生生成硫酸钡沉淀和水的反应,离子反应为Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O,故A正确;
B.BC段发生酸碱中和,离子方程式为H++OH-=H2O,故B正确;
C.CD段发生偏铝酸根离子与酸的反应,离子反应为AlO2-+H++H2O=Al(OH)3↓,故C正确;
D.DE段发生氢氧化铝与酸的反应生成硫酸铝,为强酸弱碱盐,水解使溶液显酸性,故D错误;
故选D.
A.由图象可知,AB段发生生成硫酸钡沉淀和水的反应,离子反应为Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O,故A正确;
B.BC段发生酸碱中和,离子方程式为H++OH-=H2O,故B正确;
C.CD段发生偏铝酸根离子与酸的反应,离子反应为AlO2-+H++H2O=Al(OH)3↓,故C正确;
D.DE段发生氢氧化铝与酸的反应生成硫酸铝,为强酸弱碱盐,水解使溶液显酸性,故D错误;
故选D.

练习册系列答案
相关题目

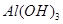 、
、