题目内容
【题目】化合物AX3和单质X2在一定条件下反应可生成化合物AX5。回答下列问题:
(1)已知AX3的熔点和沸点分别为-93.6 ℃和76 ℃,AX5的熔点为167 ℃。室温时AX3与气体X2反应生成1 mol AX5,放出热量123.8 kJ。该反应的热化学方程式为__________________________。
(2)反应AX3(g)+X2(g)![]() AX5(g)在容积为10 L的密闭容器中进行。起始时AX3和X2均为0.2mol。反应在不同条件下进行,反应体系总压强随时间的变化如图所示。
AX5(g)在容积为10 L的密闭容器中进行。起始时AX3和X2均为0.2mol。反应在不同条件下进行,反应体系总压强随时间的变化如图所示。
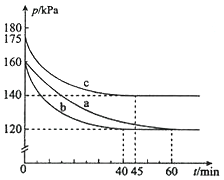
①实验a从反应开始至达到平衡时的反应速率v(AX5)=________(保留两位有效数字)。
②图中3组实验从反应开始至达到平衡时的反应速率v(AX5)由大到小的次序为___________ (填实验序号);与实验a相比,其他两组改变的实验条件及判断依据是:
b____________________、c____________________。
③用p0表示开始时总压强,p表示平衡时总压强,α表示AX3的平衡转化率,则α的表达式为__________________。
【答案】AX3(l)+X2(g)![]() AX5(s) ΔH=-123.8 kJ/mol0. 00017(或1.7×10-4 mol·L-1·min-1)bca加入催化剂,反应速率加快,但平衡没有改变温度升高,反应速率加快,但平衡向逆反应方向移动(或反应容器的容积和起始物质的量未改变,但起始总压强增大)2(1-
AX5(s) ΔH=-123.8 kJ/mol0. 00017(或1.7×10-4 mol·L-1·min-1)bca加入催化剂,反应速率加快,但平衡没有改变温度升高,反应速率加快,但平衡向逆反应方向移动(或反应容器的容积和起始物质的量未改变,但起始总压强增大)2(1-![]() )
)
【解析】
(1) 因为AX3的熔点和沸点分别为-93.6℃和76℃,AX5的熔点为167℃,室温时,AX3为液态,AX5为固态,生成1molAX5,放出热量123.8kJ,该反应的热化学方程为:AX3(l)+X2(g)=AX5(s)△H=-123.8kJmol-1,因此,本题正确答案是:AX3(l)+X2(g)=AX5(s)△H=-123.8kJmol-1;
(2) ①起始时AX3和X2均为0.2mol,即no=0.4mol,总压强为160KPa,平衡时总压强为120KPa,设平衡时总物质的量为n,根据压强之比就等于物质的量之比有 n=0.30mol。根据反应进行如下计算: 设生成AX5的量为x,
AX3(l) + X2(g)= AX5(s)
初始 (mol) 0.20 0.20 0
平衡 (mol) 0.20-x 0.20-x x
(0.20-x)+(0.20-x)+x=0.30,则x=0.10,所以实验a从反应开始至达到平衡时的反应速率v(AX5)=0.10/(10×60)=0.00017 mol·L-1·min-1)综上所述,本题答案是:0.00017(或1.7×10-4 mol·L-1·min-1)。
②根据到abc达平衡用时的多少可以比较出反应速率的大小为:b>c>a;对于曲线b,加入催化剂,反应速率加快,但平衡没有改变,压强保持不变;对于曲线c,温度升高,反应速率加快,但平衡向逆反应方向移动,压强增大(或反应容器的容积和起始物质的量未改变,但起始总压强增大) ;综上所述,本题答案是:bca;加入催化剂,反应速率加快,但平衡没有改变 ;度升高,反应速率加快,但平衡向逆反应方向移动(或反应容器的容积和起始物质的量未改变,但起始总压强增大) 。
③用p0表示开始时总压强,p表示平衡时总压强,α表示AX3的平衡转化率,根据压强之比等于物质的量之比有: p0/p=0.4/n, n=0.4×p/p0 ,据反应进行如下计算:
AX3(l) + X2(g)= AX5(s)
初始 (mol) 0.20 0.20 0
平衡 (mol) 0.20-x 0.20-x x
(0.20-x)+(0.20-x)+x=n,x=0.4-n=0.4-0.4×p/p0 = 2(1-![]() );综上所述,本题答案是:2(1-
);综上所述,本题答案是:2(1-![]() )。
)。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案