题目内容
【题目】将0.6molA和0.5molB充入0.4L密闭容器中发生2A(g)+B(g)![]() mD(g)+E(g),经过5min后达到化学平衡,此时测得D为0.2mol。又知5min内用E表示的平均反应速率为0.1mol·L-1·min-1,计算:
mD(g)+E(g),经过5min后达到化学平衡,此时测得D为0.2mol。又知5min内用E表示的平均反应速率为0.1mol·L-1·min-1,计算:
(1)m的值___________;
(2)平衡时B的转化率____________;
(3)起始与平衡时密闭容器中的压强之比_____________。
【答案】1 40% 11:9
【解析】
(1)υ(E)=0.1mol·L-1·min-1,5min内生成E的物质的量是0.1 mol·L-1·min-1×0.4L×5min=0.2mol,n(D):n(E)= 0.2mol:0.2mol=m:1,则m=1;
(2)用三段式
2A(g) + B (g)![]() D (g) + E (g)
D (g) + E (g)
起始量(mol) 0.6 0.5 0 0
转化量(mol) 0.4 0.2 0.2 0.2
平衡量(mol ) 0.2 0.3 0.2 0.2
B的转化率为![]() ×100%= 40%;
×100%= 40%;
(3)平衡时混合气总物质的量为0.2mol + 0.3mol + 0.2mol + 0.2mol=0.9mol,起始时混合气总物质的量为0.6mol + 0.5mol =1.lmol,由于容器的容积不变,所以起始与平衡时容器内的压强之比等于气体物质的量之比,故起始与平衡时密闭容器中的压强之比11 : 9。
【点晴】
本题考查化学平衡的有关计算,比较基础。有关化学平衡的计算常常使用三段式解题,要正确理解和灵活运用三段式法在化学平衡计算中的应用。

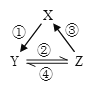
【题目】X、Y、Z 是中学化学中常见的三种物质,下表各组物质之间通过一步反应不能实现右图所示转化关系的是
X | Y | Z | 箭头上所标数字的反应条件 | ||
A. | NO | NO2 | HNO3 | ①常温遇氧气 |
|
B. | Cl2 | NaClO | HClO | ②通入CO2 | |
C. | Na2O2 | NaOH | NaCl | ③加入H2O2 | |
D. | Al2O3 | NaAlO2 | Al(OH)3 | ④加NaOH溶液 |
A. A B. B C. C D. D