题目内容
9.下列实验操作与实验目的都正确的是( )| 实验操作 | 实验目的 | |
| A | 制乙炔时用饱和食盐水代替水 | 加快化学反应速率 |
| B | CH4与SO2混合气体通过盛有溴水的洗气瓶 | 除去中CH4的SO2 |
| C | 淀粉溶液水解后冷却至室温,加新制氢氧化铜悬浊液观察现象 | 检验淀粉是否水解 |
| D | 将浓硫酸、乙醇混合加入试管中,加热,然后将导管末端插入酸性KMnO4溶液中,观察现象; | 检验是否有乙烯生成 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.将食盐水中水作溶质、食盐作溶剂,则食盐水中水的浓度降低,浓度越低,反应速率越慢;
B.二氧化硫具有还原性,能和溴发生氧化还原反应,甲烷和溴不反应;
C.葡萄糖和新制氢氧化铜悬浊液发生氧化反应需要在碱性条件下;
D.乙醇能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色.
解答 解:A.将食盐水中水作溶质、食盐作溶剂,则食盐水中水的浓度降低,浓度越低,反应速率越慢,所以用饱和食盐水代替水而减缓电石制取乙炔的反应速率,故A错误;
B.二氧化硫具有还原性,能和溴发生氧化还原反应生成硫酸和氢溴酸,甲烷和溴不反应,所以可以用溴水除去甲烷中二氧化硫,故B正确;
C.葡萄糖和新制氢氧化铜悬浊液发生氧化反应需要在碱性条件下,否则实验不成功,所以检验淀粉是否水解时应该先加入NaOH中和酸,然后再加入新制氢氧化铜悬浊液,故C错误;
D.乙醇能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色,乙醇具有挥发性,制取的乙烯中含有乙醇,要检验乙烯的生成应该先用水除去乙醇,故D错误;
故选B.
点评 本题考查化学实验方案评价,为高考高频点,涉及物质检验、反应速率的影响因素等知识点,明确实验原理是解本题关键,A采用逆向思维方法判断,注意C要在碱性条件下发生氧化反应,注意D中乙醇的干扰,这些都是易错点.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
19.若NA表示阿伏伽德罗常数,下列说法正确的是( )
| A. | 通常状况下14gN2中含有电子的数目为7NA | |
| B. | 标准状况下,22.4L水中含有水分子的数目为NA | |
| C. | 1molFe与足量稀盐酸反应时,转移电子的数目为3NA | |
| D. | 数目为NA的一氧化碳分子和0.5mol甲烷的质量比为7:4 |
20.下列解释事实的方程式不正确的是( )
| A. | 醋酸溶液显酸性:CH3COOH?H++CH3COO- | |
| B. | 用氨水除去烟气中的SO2:SO2+2NH3•H2O=(NH4)2SO3+H2O | |
| C. | 向盐碱地中施放硫酸钙,降低其碱性:Na2CO3+CaSO4=CaCO3+Na2SO4 | |
| D. | 用三氯化铁溶液腐蚀线路板:Fe3++Cu=Fe2++Cu2+ |
4.在苯的同系物中,加入少量酸性高锰酸钾溶液,振荡后溶液褪色,下列解释正确的是( )
| A. | 苯的同系物中碳原子数比苯分子中碳原子数多 | |
| B. | 苯环被KMnO4所氧化而破坏 | |
| C. | 侧链受苯环的影响而易被氧化 | |
| D. | 苯环和侧链相互影响,同时被氧化 |
14.已知莽草酸结构简式如图所示.下列说法正确的是( )


| A. | 该分子中含有2种官能团 | |
| B. | 可与FeCl3溶液作用显紫色 | |
| C. | 1 mol莽草酸可与4 mol NaOH或2molBr2完全反应 | |
| D. | 在一定条件下,该物质既可发生加成反应也可发生取代反应 |
1.已知碳碳单键可以绕键轴自由旋转,结构简式为如图所示的烃,下列说法中正确的是( )
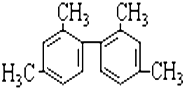

| A. | 分子中至少有9个碳原子处于同一平面上 | |
| B. | 分子中至少有10个碳原子处于同一平面上 | |
| C. | 分子中至少有11个碳原子处于同一平面上 | |
| D. | 该烃属于苯的同系物 |
18.下列有机物命名正确的是( )
| A. | 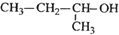 2-甲基-1-丙醇 2-甲基-1-丙醇 | B. |  3-乙基-1-丁烯 3-乙基-1-丁烯 | ||
| C. |  2-甲基-2,4-己二烯 | D. | 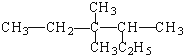 3,4,4-三甲基己烷 |
 .
.