题目内容
【题目】金属及其化合物在生产中用途广泛。
Ⅰ利用生产硼砂的废渣一一确镁泥(主要成分为MgCO3.SiO2,还含有少量Fe2O3、MnO、CaO等)为主要原料制取轻质碳酸镁[MgCO3:Mg(OH)2:2H2O]的工业流程如下:
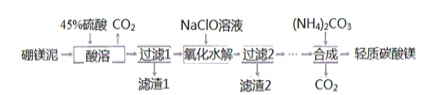
(1)写出“酸溶"一步中,MgCO3和硫酸反应的离子方程式________________________。
(2)滤渣2的主要成分有MnO2和____,写出生成MnO2的离子方程式_____________。
(3)“合成”时需通蒸汽至80℃,边加热边搅拌,温度不能超80℃的原因是________。
II.从含铜丰富的自然资源黄铜矿(CuFeS2)冶炼铜的工艺流程如下:
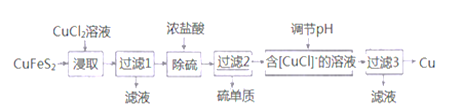
已知:①CuFeS2+3CuCl2=4CuCl↓+FeCl2+2S↓ ②+1价的Cu在酸性条件下易歧化
(4)浸取时,若改用FeCl3溶液,也能生成CuCl和S,该反应化学方程式为_______________。
(5)若过滤1所得滤液中只含FeCl2,则将其在空气中加热蒸干、灼烧后,所得固体的化学式为__________。
(6)调节溶液的pH后,除生成Cu外,还能产生一种金属离子,此金属离子是______。(填离子符号)
【答案】MgCO3+2H+=Mg2++H2O+CO2↑ Fe(OH)3 Mn2++ClO-+H2O=MnO2↓+2H++Cl- (NH4)2CO3 受热分解(或(NH4)2CO3![]() 2NH3↑+H2O+CO2↑) CuFeS2+3FeCl3=CuCl↓+ 4FeCl2+2S↓ Fe2O3 Cu2+
2NH3↑+H2O+CO2↑) CuFeS2+3FeCl3=CuCl↓+ 4FeCl2+2S↓ Fe2O3 Cu2+
【解析】
根据已知条件,CuFeS2加入CuCl2浸取发生CuFeS2+3CuCl2=4CuCl+FeCl2+2S,过滤后得到滤液含有FeCl2,固体含有CuCl、S,加入盐酸除硫,过滤得到滤液含有[CuCl2]-,调节溶液pH发生歧化反应生成Cu和Cu2+,过滤可得到Cu,得到滤液含有Cu2+,以此解答该题。
由制备流程可知,硼镁泥的主要成分为MgCO3、SiO2,还有少量Fe2O3、MnO、CaO等,向废渣中加硫酸时SiO2不溶解,过滤得到滤渣1为二氧化硅,NaClO具有氧化性,能将Mn2+氧化为MnO2,调节PH生成MnO2、Fe(OH)3沉淀,过滤得滤渣2为MnO2、Fe(OH)3,再经过系列除杂后所得溶液中加碳酸铵溶液,得到轻质碳酸镁;
(1)MgCO3和硫酸反应生成硫酸镁和二氧化碳,反应方程式为MgCO3+H2SO4=MgSO4+CO2↑+H2O,硫酸过量可以使碳酸镁充分溶解生成硫酸镁,故答案为:MgCO3+2H+=Mg2++H2O+CO2↑;
(2) 根据上面的分析可知滤渣2的主要成分为MnO2、Fe(OH)3,次氯酸钠能氧化锰离子生成MnO2,反应的离子方程式为Mn2++ClO-+H2O═MnO2↓+2H++Cl-,故答案为:Fe(OH)3;Mn2++ClO-+H2O═MnO2↓+2H++Cl-;
(3) “合成”时在溶液中加碳酸铵溶液,得到轻质碳酸镁、硫酸铵和水,温度过低反应速率慢,温度过高轻质碳酸镁、碳酸铵会分解,故答案为:温度过低反应速率慢,温度过高轻质碳酸镁、碳酸铵会分解,(NH4)2CO3 受热分解(或(NH4)2CO3![]() 2NH3↑+H2O+CO2↑);
2NH3↑+H2O+CO2↑);

 新编小学单元自测题系列答案
新编小学单元自测题系列答案 字词句段篇系列答案
字词句段篇系列答案【题目】利用如图所示装置进行下列实验,能得出相应实验结论的是( )

选项 | ① | ② | ③ | 实验结论 |
A | 稀盐酸 | CaCO3 | Na2SiO3溶液 | 非金属性:Cl>C>Si |
B | 浓硫酸 | 蔗糖 | Ba(NO3)2溶液 | 验证SO2与可溶性钡盐可生成白色沉淀 |
C | 浓氨水 | 生石灰 | 酚酞溶液 | 氨气的水溶液呈碱性 |
D | 浓硝酸 | Fe | NaOH溶液 | 铁和浓硝酸反应可生成NO2 |
A. A B. B C. C D. D