��Ŀ����
����ʹ�������Դ����չ����̼���á�����Ϊ��ѧ���о�����Ҫ���⡣�������״������ʵ����ȼ�ϣ�������ȼ�ϵ�ء�
��1������ˮ����ת������H2����Ҫת����Ӧ���£�
CH4(g) + H2O(g) CO(g) + 3H2(g) ��H=+206��2 kJ��mol��1
CO(g) + 3H2(g) ��H=+206��2 kJ��mol��1
CH4(g) + 2H2O(g) CO2(g) + 4H2(g) ��H=+165��0 kJ��mol��1
CO2(g) + 4H2(g) ��H=+165��0 kJ��mol��1
������Ӧ����ԭ�����е�CO��ʹ�ϳɰ��Ĵ����ж��������ȥ����ҵ�ϳ����ô���������CO��ˮ������Ӧ�����׳�ȥ��CO2��ͬʱ���Ƶõ�����������ķ������˷�Ӧ��Ϊһ����̼�任��Ӧ���÷�Ӧ���Ȼ�ѧ����ʽ�� ��
��2�������״���ԭ��CO��H2��Դ�ڣ�CH4(g) + H2O(g)  CO(g) + 3H2(g) ��H>0
CO(g) + 3H2(g) ��H>0
��һ��������CH4��ƽ��ת�������¶ȡ�ѹǿ�Ĺ�ϵ��ͼa����A��B��C���㴦��Ӧƽ�ⳣ����KA��KB��KC���Ĵ�С��ϵΪ___________��(�<������>������="��" )��
��100��ʱ����1 mol CH4��2 mol H2Oͨ���ݻ�Ϊ1 L�Ķ����ܷ������У�������Ӧ����˵���÷�Ӧ�Ѿ��ﵽƽ��״̬����__________
a�������������ܶȺ㶨
b����λʱ��������0��1 mol CH4ͬʱ����0��3 mol H2
c��������ѹǿ�㶨
d��3v��(CH4) = v��(H2)
��3��25��ʱ����20mL0��1mol/L������м���VmL0��1mol/LNaOH��Һ����û����Һ��pH�仯������ͼ��ʾ������˵����ȷ����_____��
A��pH��3��HF��Һ��pH��11��NaF��Һ�У� ��ˮ�������c(H+)���
B���ٵ�ʱpH��6����ʱ��Һ�У�c(F��)��c(Na+)��9��9��10-7mol/L
C���ڵ�ʱ����Һ�е�c(F��)��c(Na+)
D���۵�ʱV��20mL����ʱ��Һ��c(Na+)��0��1mol/L
��4������������һֱ��Ϊ���ĺ�������ڡ�1971��������ѧ���÷���ͨ��ϸ��ĩʱ���HFO����ṹʽΪH��O��F��HFO��ˮ��Ӧ�õ�HF�ͻ�����A���÷�Ӧ�Ļ�ѧ����ʽΪ ��
��1�� CO(g) + H2O(g) CO2(g) + H2(g) ��H=��41��2 kJ��mol��1 ��2�֣�
CO2(g) + H2(g) ��H=��41��2 kJ��mol��1 ��2�֣�
��2���� KC = KB >KA ��2�֣�
�� cd ��2�֣�
��3��BC ��2�֣�
��4��H2O��HFO=HF��H2O2 ��2�֣�
���������������1�� �ȶ���֪�Ȼ�ѧ����ʽ���Ϊ�٢ڣ��۲췢�֢�-�ٿɵã�CO(g) + H2O(g) CO2(g) + H2(g) ��H=��41��2 kJ��mol��1��
CO2(g) + H2(g) ��H=��41��2 kJ��mol��1��
��2���� ƽ�ⳣ��ָ��������Ũ�ȵĻ�ѧ���������ݵij˻����Ը���Ӧ��Ũ�ȵĻ�ѧ���������ݵij˻����õı�ֵ����ѧƽ�ⳣ��ֻ���¶��йأ�����B��C��������ͬ���¶ȣ�����KC = KB��Ȼ��A��B������ȣ���A��B�������ת���ʱ��˵���������ƶ�����ѧƽ�ⳣ���������KB>KA �����Դ���KC = KB >KA��
�� ��������������ֲ��䣬���������غ㶨��֪����Ӧǰ����������������䣬����������������ܶȲ��䣬���Բ��ܱ����ﵽ��ѧƽ��״̬����a����λʱ��������0��1 mol CH4ͬʱ����0��3 mol H2��������v�������Բ��ܱ����ﵽ��ѧƽ��״̬����b�����淴Ӧ���л�����������ʵ������������ݻ����䣬ѹǿ����������ѹǿ�㶨ʱ��˵������ƽ�⣬��c��ȷ��3v��(CH4) = v��(H2)�����ʵ���������֮�ȵ��ڻ�ѧ������֮�ȣ���Ӧ����ƽ�⣬��d��ȷ������ѡcd��
��3��pH��3��HF��Һ����ˮ�������c(H+)�� ��10-11mol��L��1��pH��11��NaF��Һ�У���ˮ�������c(H+)��10-14/10-11��10-3mol��L��1��A�����ٵ�ʱ�����ݵ����غ㣬c(OH��)��c(F��)��c(Na+)��c(H��)��c(F��)��c(Na+)��c(H��)��c(OH��)��10-6��
��10-11mol��L��1��pH��11��NaF��Һ�У���ˮ�������c(H+)��10-14/10-11��10-3mol��L��1��A�����ٵ�ʱ�����ݵ����غ㣬c(OH��)��c(F��)��c(Na+)��c(H��)��c(F��)��c(Na+)��c(H��)��c(OH��)��10-6�� ��9��9��10-7mol/L��B�ԣ����ݵ����غ㣬c(OH��)��c(F��)��c(Na+)��c(H��)���ڵ�ʱpH=7����Һ�е�c(H��)��c(OH��)������c(F��)��c(Na+)��C�ԣ��۵�ʱV��20mL����ʱ��Һ��c(Na+)��
��9��9��10-7mol/L��B�ԣ����ݵ����غ㣬c(OH��)��c(F��)��c(Na+)��c(H��)���ڵ�ʱpH=7����Һ�е�c(H��)��c(OH��)������c(F��)��c(Na+)��C�ԣ��۵�ʱV��20mL����ʱ��Һ��c(Na+)�� ��0��05mol/L������ѡBC��
��0��05mol/L������ѡBC��
��4���縺��F��O����H-O-F��FԪ�ر���-1�ۣ���ˮ��Ӧ����HF������ˮ�ⷴӦ������֪AΪH-O-O-H���÷�Ӧ�Ļ�ѧ����ʽΪ��H2O+HFO=HF+H2O2��
���㣺�����Ȼ�ѧ����ʽ����ѧƽ��ͼ��Ӱ�����ء�ƽ�ⳣ����ƽ��״̬�жϡ�������ʵĵ��롢����Ũ�ȱȽϵȡ�

X��Y��Z��W��Ϊ10���ӵķ��ӻ����ӡ�X��5��ԭ�Ӻˡ�ͨ��״���£�WΪ��ɫҺ�塣����֮��ת����ϵ��ͼ��ʾ����ش�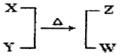
��1����ҵ��ÿ��ȡ1molZҪ�ų�46.2 kJ��������д���÷�Ӧ���Ȼ�ѧ����ʽ�� ��
��2����ҵ��ȡZ�Ļ�ѧƽ�ⳣ��K��T�Ĺ�ϵ���±���
| T/K | 298 | 398 | 498 | ���� |
| K/(mol��L��1)��2 | 4.1��106 | K1 | K2 | ���� |
������������⣺
���ԱȽ�K1��K2�Ĵ�С��K1 K2����д��>����=����<����
�ں��¹̶�����������У����и�������Ϊ�жϸ÷�Ӧ�ﵽ��ѧƽ��״̬�����ݵ��� ���������ĸ����
A�������ڸ����ʵ�Ũ��֮��Ϊ��ѧ��������
B����������ܶȱ��ֲ���
C��������ѹǿ���ֲ���
D�����������Է����������ֲ���
��3��ij��ѧС��ͬѧģ�ҵ������ȡHNO3�������ͼ��ʾװ�ã�����aΪһ���ɳ��������������Ƥ��
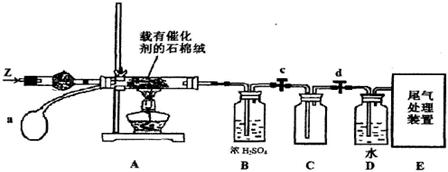
��A�з�����Ӧ�Ļ�ѧ����ʽ�� ��
��B��ŨH2SO4�������� ��
��4��д��Dװ���з�Ӧ�Ļ�ѧ����ʽ ��
��5��a��ͨ����������� ��
ú��������úΪԭ��,������ѧ�ӹ�ʹúת��Ϊ���塢Һ�塢����ȼ���Լ����ֻ�����Ʒ�Ĺ�ҵ���̡�
(1)��֪��25 �桢101 kPaʱ,C(s)��H2(g)��CO(g)ȼ�յ��Ȼ�ѧ����ʽ�ֱ�Ϊ:
C(s)+O2(g) CO2(g)����H1="-393.5" kJ/mol;
CO2(g)����H1="-393.5" kJ/mol;
H2(g)+ O2(g)
O2(g) H2O(g)����H2="-241.8" kJ/mol;
H2O(g)����H2="-241.8" kJ/mol;
CO(g)+ O2(g)
O2(g) CO2(g)����H3="-283.0" kJ/mol;
CO2(g)����H3="-283.0" kJ/mol;
����C(s)+H2O(g) CO(g)+H2(g)����H=��������,�÷�Ӧƽ�ⳣ���ı���ʽΪK=��������������������;�����¶�,��Kֵ��������(��������С�����䡱)��
CO(g)+H2(g)����H=��������,�÷�Ӧƽ�ⳣ���ı���ʽΪK=��������������������;�����¶�,��Kֵ��������(��������С�����䡱)��
������ٷ�Ӧ���ݻ�������ܱ������н���,����Ӧ�ﵽƽ��ʱ��������(����)��
a.v��(CO)��v��(H2)=1��1
b.̼���������ֲ���
c.v��(CO)=v��(H2O)
d.�����е�ѹǿ����
�����ݻ�������ܱ������н��Тٷ�Ӧ,����ʹc(CO)�����������������
a.�����¶�
b.����He(g),ʹ��ϵѹǿ����
c.��H2(g)����ϵ�з������
d.�������
(2)����ͬ����CO(g)��H2O(g)�ֱ�ͨ�����Ϊ2 L�ĺ����ܱ�������,���з�ӦCO(g)+H2O(g) CO2(g)+H2(g),�õ�����2������:
CO2(g)+H2(g),�õ�����2������:
| ʵ���� | �¶�/�� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ���� ��ʱ��/min | ||
| H2O | CO | H2 | CO | |||
| 1 | 650 | 2 | 4 | 1.6 | 2.4 | 5 |
| 2 | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
����ʵ��2��ƽ���������ټ���0.4 mol H2O(g)��0.4 mol CO2,�ﵽ��ƽ��ʱCO��ת������������(��������С�����䡱)��
�µġ���������������������2016��1��1�����ҹ�ȫ��ʵʩ���ݴˣ�������������ָ��(AQI)�ձ���ʵʱ���������SO2��NO2��CO��O3��PM10��PM2.5��ָ�꣬Ϊ�����ṩ����ָ�����������ؾ���������ų��к����
(1)�����ų���β���к���CO��NO�����壬�û�ѧ����ʽ���Ͳ���NO��ԭ��________________________________________
(2)�����������ڰ�װ�Ĵ�ת��������ʹ����β���е���Ҫ��Ⱦ��ת��Ϊ���Ĵ���ѭ�����ʡ���֪��
N2(g)��O2(g)===2NO(g)����H����180.5 kJ��mol��1
2C(s)��O2(g)===2CO(g)����H����221.0 kJ��mol��1
C(s)��O2(g)===CO2(g)����H����393.5 kJ��mol��1
��Ӧ2NO(g)��2CO(g)??N2(g)��2CO2(g)�Ħ�H��________kJ��mol��1���÷�Ӧ�Ħ�S________0(�>����<������)��
(3)��0.20 mol NO��0.10 mol CO����һ���ݻ��㶨Ϊ1 L���ܱ������У��ڲ�ͬ�����·�Ӧ�����в������ʵ�Ũ�ȱ仯״����ͼ��ʾ��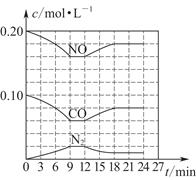
�ټ������N2��6��9 minʱ��ƽ����Ӧ����v(N2)��________mol��L��1��min��1��
�ڵ�12 minʱ�ı�ķ�Ӧ����Ϊ________(����¡����¡�)��
�ۼ��㷴Ӧ�ڵ�24 minʱ��ƽ�ⳣ��K��________���������¶Ȳ��䣬���������г���CO��N2��0.060 mol��ƽ�⽫________�ƶ�(�����������)��
(4)��������л����ó������ⶨ�����к��нϸ�Ũ��SO2�ĺ����������һЩ������20 ����������±���
| �ܽ��(S)/g | �ܶȻ�(Ksp) | ||
| Ca(OH)2 | Ba(OH)2 | CaSO3 | BaSO3 |
| 0.160 | 3.89 | 6.76��10��3 | 5.48��10��9 |
������SO2����ʵ��Լ���________[�Ca(OH)2����Ba(OH)2��]��Һ��
����20 ��ʱ����CaSO3����Һ�еμ�������BaCl2��Һ����CaSO3��BaSO3��ת���ﵽƽ��ʱ����Һ�е�
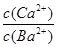 ��____________(д������ʽ����)��
��____________(д������ʽ����)�� �ҹ��Ǹ��������,��������Ϊ�����һ,��¯��������Ϊ�ձ������������
I.��֪��Ӧ  Fe2O3(s)+ CO(g)
Fe2O3(s)+ CO(g)
 Fe(s)+ CO2(g) ��H��-23.5 kJ��mol-1���÷�Ӧ��
Fe(s)+ CO2(g) ��H��-23.5 kJ��mol-1���÷�Ӧ��
1000���ƽ�ⳣ������4����һ���ݻ�Ϊ10L���ܱ�������,1000��ʱ����Fe��Fe2O3��CO��CO2��1. 0mol,��Ӧ����l0min��ﵽƽ�⡣
��1��CO��ƽ��ת����=____________
��2�������CO��ƽ��ת����,�ٽ�Fe2O3��ת��,�ɲ�ȡ�Ĵ�ʩ��________
a����߷�Ӧ�¶�
b������Ӧ��ϵ��ѹǿ
c��ѡȡ���ʵĴ���
d����ʱ���ջ��Ƴ�����CO2
e�������ʯ,ʹ����ƽ���������ֽӴ�
��.��¯���������ķ����е�CO�ɽ��л���,ʹ����һ�������º�H2��Ӧ�Ʊ��״�:
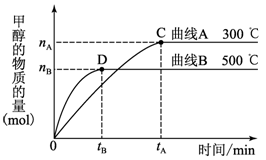
CO(g)+ 2H2(g) CH3OH(g)�������ͼʾ�ش���������:
CH3OH(g)�������ͼʾ�ش���������: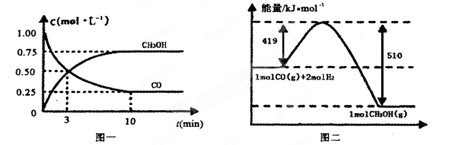
��1���ӷ�Ӧ��ʼ��ƽ��,��H2Ũ�ȱ仯��ʾƽ����Ӧ����v(H2)=________
��2�������¶Ⱥ�������ͬ�������ܱ�������,����ͬ��ʽͶ�뷴Ӧ��,��÷�Ӧ�ﵽƽ�ⅼ���й��������±���
| ���� | ��Ӧ��Ͷ����� | ��Ӧ��� ת���� | CH3OH��Ũ�� | �����仯 (Q1��Q2��Q3������0) |
| �� | 1mol CO��2mol H2 | ��1 | c1 | �ų�Q1kJ���� |
| �� | 1mol CH3OH | ��2 | c2 | ����Q2kJ���� |
| �� | 2mol CO��4mol H2 | ��3 | c3 | �ų�Q3kJ���� |
�����й�ϵ��ȷ����________
A��c1=c2 B��2Q1=Q3 C��2��1=��3 D����1+��2 =1
E���÷�Ӧ������1mol CH3OH����ų�(Q1+Q2)kJ����
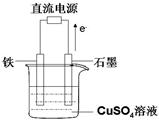
���Լ���Ϊȼ�ϵ����͵�أ���ɱ�����������Ϊȼ�ϵĴ�ͳȼ�ϵ�أ�Ŀǰ�õ��㷺���о�����ͼ��Ŀǰ�о��϶��һ�����������ȼ�ϵ�ع���ԭ��ʾ��ͼ���ش��������⣺
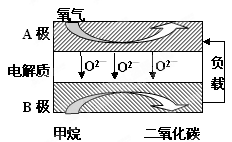
��1��B���ϵĵ缫��ӦʽΪ
��2�����ø�ȼ�ϵ������Դ����ʯī���缫���100mL 1mol/L������ͭ��Һ���������ռ���������������ʱ�����������ĵļ�������Ϊ ������£���
 H2(g)+CO2(g) ��H����41kJ��mol��1
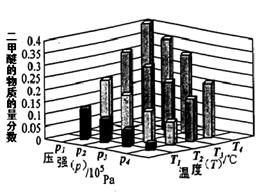
H2(g)+CO2(g) ��H����41kJ��mol��1 CH3OCH3(g) + 3H2O(g)����֪һ�������£��÷�Ӧ��CO2��ƽ��ת�������¶ȡ�Ͷ�ϱ�[n(H2) / n(CO2)]�ı仯����������ͼ��
CH3OCH3(g) + 3H2O(g)����֪һ�������£��÷�Ӧ��CO2��ƽ��ת�������¶ȡ�Ͷ�ϱ�[n(H2) / n(CO2)]�ı仯����������ͼ��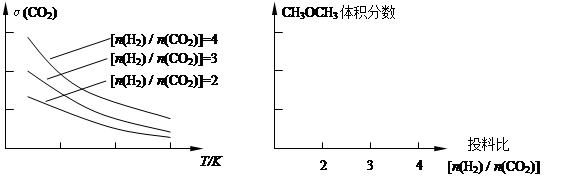
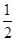 O2(g)=FeO(s)����H����272.0 kJ��mol��1
O2(g)=FeO(s)����H����272.0 kJ��mol��1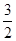 O2(g)=Al2O3(s)����H����1675.7 kJ��mol��1
O2(g)=Al2O3(s)����H����1675.7 kJ��mol��1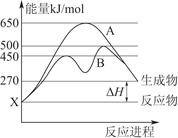
 Na2S(s)��4H2O(g)
Na2S(s)��4H2O(g)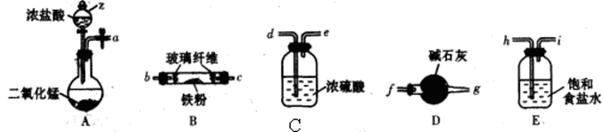
 Fe3��(aq)��3OH��(aq) ��H��a kJ/mol
Fe3��(aq)��3OH��(aq) ��H��a kJ/mol