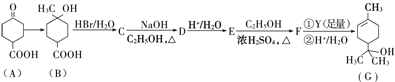��Ŀ����
����Ŀ��ij�ػ�������ȡһ����ij�������ŷ�ˮ�����ֳɼס��ҡ��������ķݣ�������ͼ��ʾ̽����

��֪��ˮ�����п��ܺ����±��е����ӣ�
������ | Na+��Mg2+��X |
������ | Cl����SO32����Y��NO3�� |
��1������X�� ���ѧʽ����ͬ��������Y�� ��
��2�����в���ȷ���Ƿ���ڵ��������� ����֤�����������Ƿ���ڵļ�ʵ�����Ϊ ��
��3������ʵ�������������·�����Ӧ�����ӷ���ʽ�� ��
���𰸡���1��NH4+��SO42����2��Cl����ȡ������ˮ�������μ�������Ba��NO3��2��Һ�����ã�ȡ�ϲ���Һ���μ������ữ��AgNO3��Һ�����а�ɫ���������������Cl�������ް�ɫ��������������Cl������3��6I��+2NO3��+8H+=2NO��+3I2+4H2O
���������⣺���м�����ˮ����ɫ��֤��������ԭ�����ӣ��ƶϲ���SO32�������м����ữ���Ȼ������ɰ�ɫ����˵������SO42�������м�������������Һ���ȷ�Ӧ��������ʹʪ��ĺ�ɫʯ����ֽ����ɫ��֤���ǰ�����˵��ԭ��Һ�к���NH4+�����м�����۵⻯����Һ����Һ����ɫ˵����Һ�к�������������������������Ϊ���ʵ⣻�жϺ���NO3����
��1������XΪNH4+������YΪSO42�����ʴ�Ϊ��NH4+��SO42����
��2�����в���ȷ���Ƿ���ڵ���������Cl������֤�����������Ƿ���ڵļ�ʵ�����Ϊ��ȡ������Һ���Թ��У�����ϡ���ᣬ�ټ�����������Һ���ɰ�ɫ����֤�������ӵĴ���Cl����
�ʴ�Ϊ��Cl����ȡ������ˮ�������μ�������Ba��NO3��2��Һ�����ã�ȡ�ϲ���Һ���μ������ữ��AgNO3��Һ�����а�ɫ���������������Cl�������ް�ɫ��������������Cl����
��3������ʵ�������������·�����Ӧ�Ƿ�ˮ�����еμӵ���һKI��Һ������Ӧ�����������������Һ�з���������ԭ��Ӧ����Ӧ�����ӷ���ʽ��6I��+2NO3��+8H+=2NO��+3I2+4H2O��
�ʴ�Ϊ��6I��+2NO3��+8H+=2NO��+3I2+4H2O��