题目内容
金属及其化合物在生产、生活中有广泛应用.请回答下列问题:
(1)工业上常利用Fe2+能与CN-形成稳定Fe(CN)4-6(六氰合亚铁离子)的特点来处理含CN-的工业废水.
①写出基态Fe2+的电子排布式______.
②从结构角度分析Fe3+较Fe2+稳定的原因______.
③CN-中C原子的杂化轨道类型为______.
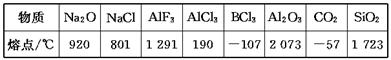
(2)三氯化铁常温下为固体,熔点282℃,沸点315℃,在300℃以上易升华.易溶于水,也易溶于乙醚、丙酮等有机溶剂.据此判断三氯化铁晶体中存在的微粒间作用力有______.
(3)铁元素为血红蛋白和肌红蛋白的活性部分--血红素的重要组成部分;
①血红素的结构式为:
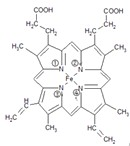
血红素中含有C、H、O、N、Fe五种元素,C、N、O三种元素的第一电离能由小到大的顺序是______.铁原子周围哪些氮原子参与形成了配位键______(空格上填氮原子标号).
(4)钙是人体所需的重要元素之一,有一种补钙剂--抗坏血酸钙的组成为Ca(C6H7O6)2?4H2O,其结构示意图如下:
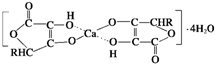
该物质中存在的化学键类型包括______(填字母).
A.金属键B.离子键 C.非极性共价键D.配位键
(5)金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好.离子型氧化物V2O5和CrO2中,适合作录音带磁粉原料的是______.
(1)工业上常利用Fe2+能与CN-形成稳定Fe(CN)4-6(六氰合亚铁离子)的特点来处理含CN-的工业废水.
①写出基态Fe2+的电子排布式______.
②从结构角度分析Fe3+较Fe2+稳定的原因______.
③CN-中C原子的杂化轨道类型为______.
(2)三氯化铁常温下为固体,熔点282℃,沸点315℃,在300℃以上易升华.易溶于水,也易溶于乙醚、丙酮等有机溶剂.据此判断三氯化铁晶体中存在的微粒间作用力有______.
(3)铁元素为血红蛋白和肌红蛋白的活性部分--血红素的重要组成部分;
①血红素的结构式为:

血红素中含有C、H、O、N、Fe五种元素,C、N、O三种元素的第一电离能由小到大的顺序是______.铁原子周围哪些氮原子参与形成了配位键______(空格上填氮原子标号).
(4)钙是人体所需的重要元素之一,有一种补钙剂--抗坏血酸钙的组成为Ca(C6H7O6)2?4H2O,其结构示意图如下:

该物质中存在的化学键类型包括______(填字母).
A.金属键B.离子键 C.非极性共价键D.配位键
(5)金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好.离子型氧化物V2O5和CrO2中,适合作录音带磁粉原料的是______.
(1)①Fe的原子序数为26,基态Fe2+的电子为24,其电子排布式为1s22s22p63s23p63d6,故答案为:1s22s22p63s23p63d6;
②Fe3+较Fe2+稳定,是因Fe3+的3d能级为3d5半充满状态,较稳定,故答案为:Fe3+的3d能级为3d5半充满状态,较稳定;
③CN-中存在C≡N,C原子杂化轨道数目为2,杂化类型为sp杂化,故答案为:sp;
(2)常温下为固体,熔点282℃,沸点315℃,在300℃以上易升华.易溶于水,也易溶于乙醚、丙酮等有机溶剂.则为分子晶体,存在极性共价键、范德华力,
故答案为:极性共价键、范德华力;
(3)①C、N、O三种元素的第一电离能中,N原子2p电子半满为稳定结构,第一电离能最大;非金属性越强,第一电离能越大,则第一电离能为N>O>C;N原子提供孤对电子形成配位键,由图可知,①④形成配位键,故答案为:C<O<N;①④;
(4)金属键存在与金属或合金中,该物质中钙离子与阴离子之间存在离子键,且钙离子与O原子形成配位键,C-C之间存在非极性共价键,即该物质存在离子键、配位键、非极性共价键,故答案为:BCD;
(5)V2O5中V的最外层电子全部失去或成键,CrO2中Cr失去4个电子,离子的最外层电子为2,为成对,离子含未成对电子越多,则磁性越大,则适合作录音带磁粉原料的是CrO2,
故答案为:CrO2.
②Fe3+较Fe2+稳定,是因Fe3+的3d能级为3d5半充满状态,较稳定,故答案为:Fe3+的3d能级为3d5半充满状态,较稳定;
③CN-中存在C≡N,C原子杂化轨道数目为2,杂化类型为sp杂化,故答案为:sp;
(2)常温下为固体,熔点282℃,沸点315℃,在300℃以上易升华.易溶于水,也易溶于乙醚、丙酮等有机溶剂.则为分子晶体,存在极性共价键、范德华力,
故答案为:极性共价键、范德华力;
(3)①C、N、O三种元素的第一电离能中,N原子2p电子半满为稳定结构,第一电离能最大;非金属性越强,第一电离能越大,则第一电离能为N>O>C;N原子提供孤对电子形成配位键,由图可知,①④形成配位键,故答案为:C<O<N;①④;
(4)金属键存在与金属或合金中,该物质中钙离子与阴离子之间存在离子键,且钙离子与O原子形成配位键,C-C之间存在非极性共价键,即该物质存在离子键、配位键、非极性共价键,故答案为:BCD;
(5)V2O5中V的最外层电子全部失去或成键,CrO2中Cr失去4个电子,离子的最外层电子为2,为成对,离子含未成对电子越多,则磁性越大,则适合作录音带磁粉原料的是CrO2,
故答案为:CrO2.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
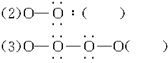

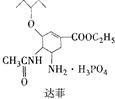
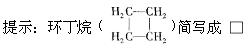
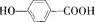 ),B在浓硫酸加热作用下可得到缩聚物C,C的结构简式是______________;水杨酸是一种与B具有相同官能团的同分异构体,且苯环上的取代基相邻,请写出水杨酸与乙酸酐合成阿司匹林(乙酰水杨酸)的化学方程式(有机物用结构简式表示):______________________________________;B的同分异构体中既含有酚羟基又含有酯基的共有三种,写出其中一种同分异构体的结构简式 _________________________。
),B在浓硫酸加热作用下可得到缩聚物C,C的结构简式是______________;水杨酸是一种与B具有相同官能团的同分异构体,且苯环上的取代基相邻,请写出水杨酸与乙酸酐合成阿司匹林(乙酰水杨酸)的化学方程式(有机物用结构简式表示):______________________________________;B的同分异构体中既含有酚羟基又含有酯基的共有三种,写出其中一种同分异构体的结构简式 _________________________。