题目内容
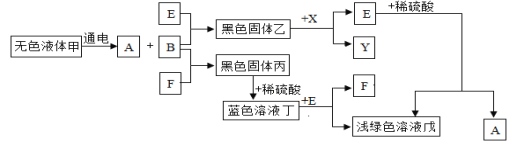
【题目】现有NH3、CO、Na、Na2O2、Fe、NO、NO2、F2、SO2、SOCl2等物质,根据它们的组成及性质进行如下分类:

请回答下列问题:
(1)图中所示的分类方法叫___________。
(2)淡黄色固体最终位于__________组,它的电子式为___________。
(3)B组中有一种物质在高温下能与水蒸气反应,若该反应过程中有8×6.02×1023个电子转移,则有__g该物质参与反应。
(4)C组有一种气体常用作工业上冶炼铁的还原剂,写出高温下它还原Fe2O3的化学方程式___________。
(5)II组某种物质能与水发生氧化还原反应,该反应中被氧化元素与被还原的元素的质量比为___________。
(6)II组另有一种物质滴入水中后与水剧烈反应,元素化合价不发生变化,该物质与水反应的化学方程式___________。
【答案】树状分类法 I组  168 3CO+Fe2O3
168 3CO+Fe2O3![]() 3CO2+2Fe 2:1 SOCl2+H2O =SO2+2HCl
3CO2+2Fe 2:1 SOCl2+H2O =SO2+2HCl
【解析】
按照不同的标准,给物质分类。
(1)由分类的角度可知为树状分类法;
(2)淡黄色固体为Na2O2,可与水反应生成NaOH和氧气;过氧化钠为离子化合物,据此书写电子式;
(3)B组中与水在高温条件下反应的物质为Fe,根据反应方程式分析;
(4)依据高炉炼铁原理,一氧化碳与氧化铁反应生成铁和二氧化碳解答;
(5)Ⅱ组的某种物质能与水发生氧化还原反应生成酸,该物质为NO2,据此书写离子方程式;
(6)根据化合价不变,推测出产物,再根据原子守恒写出方程式。
物质按照组成物质的元素种类分类,Na、Fe、F2为一组,只由一种元素组成,能够和H2化合的为F2,则A组中有F2,B组中Na和Fe;乙组中均为化合物,能够与水反应的有CO、NO,则C组中有CO和NO。能够与水反应的中,生成碱的有NH3和Na2O2;则Ⅰ组中有NH3和Na2O2。Ⅱ组中有NO2、SO2、SOCl2。
(1)图示方法将多种单质和化合物按照层次,一层一层来分,符合树状分类的特点,属于树状分类;
(2)淡黄色固体为Na2O2,可与水反应生成NaOH和氧气,最终位于I组;Na2O2是钠离子和过氧根离子构成的离子化合物,电子式为 ;
;
(3)B组中Fe可以在高温下与水蒸气发生反应;化学方程式为3Fe+4H2O(g)![]() Fe3O4+4H2;若该反应过程中有8×6.02×1023个电子转移,即转移8mol电子,则消耗3molFe,即3mol×56g·mol-1=168g;
Fe3O4+4H2;若该反应过程中有8×6.02×1023个电子转移,即转移8mol电子,则消耗3molFe,即3mol×56g·mol-1=168g;
(4)C组有一种气体常用作工业上冶炼铁的还原剂是CO,CO与Fe2O3的反应方程式为3CO+Fe2O3 ![]() 3CO2+2Fe;
3CO2+2Fe;
(5)Ⅱ组的某种物质能与水发生氧化还原反应,该物质为NO2,二氧化氮与水反应生成硝酸和一氧化氮,化学方程式为3NO2+H2O=2HNO3+NO;3molNO2中化合价升高的N有2mol,化合价降低的N有1mol;则被氧化的NO2有2mol,被还原的NO2有1mol,比例为2:1;
(6)Ⅱ组另有一种物质滴入水中后与水激烈反应,该物质为SOCl2,其化合价不变,S的化合价为+4,则生成SO2,Cl的化合价为-1,生成HCl。化学方程式为SOCl2+H2O =SO2+2HCl。