题目内容
13.已知298.15K时,可逆反应:Pb2+(aq)+Sn(s)?Pb(s)+Sn2+(aq)的平衡常数K=2.2,若溶液中Pb2+和Sn2+的浓度均为0.10mol•L-1,则此时反应进行的方向是( )| A. | 向正反应方向进行 | B. | 向逆反应方向进行 | ||
| C. | 处于平衡状态 | D. | 无法判断 |
分析 计算此时溶液浓度商,和平衡常数比较判断反应进行的方向.
解答 解:已知298.15K时,可逆反应:Pb2+(aq)+Sn(s)?Pb(s)+Sn2+(aq)的平衡常数K=2.2,若溶液中Pb2+和Sn2+的浓度均为0.10mol•L-1,Qc=$\frac{c(S{n}^{2+})}{c(P{b}^{2+})}$=1<K=2.2,反应正向进行,
A、上述计算分析可知,反应正向进行,故A正确;
B、反应正向进行,故B错误;
C、反应为达到平衡状态,故C错误;
D、依据浓度商和平衡常数比较大小,可以分析判断反应进行的分析,故D错误;
故选A.
点评 本题考查了化学平衡的影响因素分析判断,浓度商和平衡常数的计算应用,掌握基础是解题关键,题目较简单.

练习册系列答案
相关题目
3.下列解释物质用途或现象的反应方程式不准确的是( )
| A. | 硫酸型酸雨的形成会涉及反应:2H2SO3+O2$\frac{\underline{\;催化剂\;}}{\;}$2H2SO4 | |
| B. | 工业上制取粗硅的化学方程式:SiO2+C$\frac{\underline{\;高温\;}}{\;}$Si+CO2↑ | |
| C. | Na2 S203溶液中加入稀硫酸:S2O+2H${\;}_{3}^{2-}$═SO2+S↓+HO2 | |
| D. | 成分为盐酸的洁厕灵与84消毒液混合使用易中毒:Cl-+ClO-+2H+═Cl2↑+H20 |
4.浅绿色的硝酸亚铁溶液存在如下平衡 Fe2++2H2O?Fe(OH)2+2H+在溶液中加入盐酸后.溶液变( )
| A. | Fe2+浓度增大,绿色变深 | B. | 加盐酸后体积增大,绿色变浅 | ||
| C. | 溶液变棕黄色 | D. | 溶液颜色基本不变 |
1.NA为阿伏加德罗常数,下列叙述错误的是( )
| A. | 18gH2O中含有的质子数为10NA | |
| B. | 7.1gCl2与足量氢氧化钠溶液反应转移电子数为0.2NA | |
| C. | 46gNO2和N2O4混合气体中含有原子总数为3NA | |
| D. | 1molNa与足量O2反应,生成Na2O和Na2O2的混合物,钠失0NA个电子 |
8.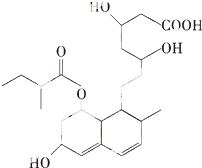 普伐他汀是一种调节血脂的药物,其结构如图所示(未表示出其空间构型).下列关于普伐他汀的性质描述不正确的是( )
普伐他汀是一种调节血脂的药物,其结构如图所示(未表示出其空间构型).下列关于普伐他汀的性质描述不正确的是( )
 普伐他汀是一种调节血脂的药物,其结构如图所示(未表示出其空间构型).下列关于普伐他汀的性质描述不正确的是( )
普伐他汀是一种调节血脂的药物,其结构如图所示(未表示出其空间构型).下列关于普伐他汀的性质描述不正确的是( )| A. | 3个-OH皆可发生催化氧化反应 | |
| B. | 能使酸性KMnO4溶液褪色 | |
| C. | 能发生加成、取代、消去反应 | |
| D. | 1 mol该物质最多可与1mol NaOH反应 |
18.下列说法中正确的是( )
| A. | 将322 gNa2SO4•10H2O溶于1L水中,所得溶液的物质的量浓度为1 mol•L-1 | |
| B. | 将1L2mol•L-1 H2SO4溶液加水稀释到2L,所得溶液的物质的量浓度为1mol•L-1 | |
| C. | 将1L18.4 mol•L-1的H2SO4溶液加入到1L水中,所得溶液的物质的量浓度为9.2mol•L-1 | |
| D. | 将336mLHCl气体溶于水,配成300mL溶液,所得溶液的物质的量浓度为0.05mol•L-1 |
5. 甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:2H2(g)+CO(g)═CH3OH(g)
甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:2H2(g)+CO(g)═CH3OH(g)
(1)下表所列数据是该反应在不同温度下的化学平衡常数(K)
①该反应的平衡常数表达式K=$\frac{c(C{H}_{3}OH)}{{c}^{2}({H}_{2})•c(CO)}$,△H<0(填“>”、“<”或“=”).
②要提高CO的转化率,可以采取的措施是df(填序号).
a.升温
b.加入催化剂
c.增加CO的浓度
d.加入H2加压
e.加入惰性气体加压
f.分离出甲醇
③300℃时,将容器的容积压缩到原来的1/2,在其他条件不变的情况下,对平衡体系产生的影响是CD(填字母).
A.c(H2)减少 B.正反应速率加快,逆反应速率减慢
C.CH3OH 的物质的量增加 D.重新平衡时c(H2)/c(CH3OH)减小
④某温度下,将2mol CO和6mol H2充入2L的密闭容器中,充分反应10min后,达到平衡时测得c(CO)=0.2mol/L,则CO的转化率为80%,此时的温度为250℃.以CH3OH表示该过程的反应速率v(CH3OH)=0.08mol/(L•min).
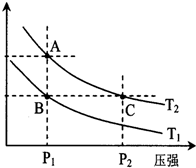
(2)下图表示在温度分别为T1、T2时,平衡体系中H2的体积分数随压强变化曲线,A、C两点的反应速率A<C(填“>”、“=”或“<”,下同),A、C两点的化学平衡常数A=C,由状态B到状态A,可采用升温的方法(填“升温”或“降温”).
(3)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H=-a kJ•mol-1
②2CO(g)+O2(g)=2CO2(g)△H=-b kJ•mol-1
③H2O(g)=H2O(l)△H=-c kJ•mol-1
则,CH3OH(l)+O2(g)=CO(g)+2H2O(l)△H=$\frac{b-a}{2}$-2ckJ•mol-1.
 甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:2H2(g)+CO(g)═CH3OH(g)
甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:2H2(g)+CO(g)═CH3OH(g)(1)下表所列数据是该反应在不同温度下的化学平衡常数(K)
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
②要提高CO的转化率,可以采取的措施是df(填序号).
a.升温
b.加入催化剂
c.增加CO的浓度
d.加入H2加压
e.加入惰性气体加压
f.分离出甲醇
③300℃时,将容器的容积压缩到原来的1/2,在其他条件不变的情况下,对平衡体系产生的影响是CD(填字母).
A.c(H2)减少 B.正反应速率加快,逆反应速率减慢
C.CH3OH 的物质的量增加 D.重新平衡时c(H2)/c(CH3OH)减小
④某温度下,将2mol CO和6mol H2充入2L的密闭容器中,充分反应10min后,达到平衡时测得c(CO)=0.2mol/L,则CO的转化率为80%,此时的温度为250℃.以CH3OH表示该过程的反应速率v(CH3OH)=0.08mol/(L•min).
(2)下图表示在温度分别为T1、T2时,平衡体系中H2的体积分数随压强变化曲线,A、C两点的反应速率A<C(填“>”、“=”或“<”,下同),A、C两点的化学平衡常数A=C,由状态B到状态A,可采用升温的方法(填“升温”或“降温”).
(3)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H=-a kJ•mol-1
②2CO(g)+O2(g)=2CO2(g)△H=-b kJ•mol-1
③H2O(g)=H2O(l)△H=-c kJ•mol-1
则,CH3OH(l)+O2(g)=CO(g)+2H2O(l)△H=$\frac{b-a}{2}$-2ckJ•mol-1.
2.下列化学用语表达正确的是( )
| A. | 小苏打电离方程式:NaHCO3+H2O?Na++H3O++CO32- | |
| B. | 丙烷分子的球棍模型: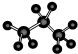 | |
| C. | 氮气化学性质稳定是因为其分子中含有氮氮三键,电子式为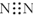 | |
| D. | 核内含有1个质子和1个中子的原子可表示为:${\;}_{1}^{1}$H |
3.一定条件下化学反应:CO2(g)+H2(g)?CO(g)+H2O(g),的化学平衡常数K=1,相同条件下,当C(CO2)=0.5mol•L-1、C(H2)=0.5mol•L-1、C(CO)=1mol•L-1、C(H2O)=1mol•L-1时,下列说法正确的是( )
| A. | 处于平衡状态,正逆反应速率相等 | |
| B. | 平衡逆移,正反应速率小于逆反应速率 | |
| C. | CO2的转化率为50% | |
| D. | 该条件下,学平衡常数K=4 |