题目内容
9.在C2H2、C6H6、C2H2O2组成的混合物中,已知氧元素的质量分数为8%,则混合物中碳元素的质量分数( )| A. | 92.3% | B. | 87.6% | C. | 75% | D. | 84.9% |
分析 C2H2、C6H6、C2H2O2中C、H原子数目之比均为1:1,即混合物中C、H元素质量之比为12:1,根据O氧元素质量分数计算混合物中C、H元素总质量分数,再根据C、H元素质量之比计算碳元素质量分数.
解答 解:C2H2、C6H6、C2H2O2中C、H原子数目之比均为1:1,即混合物中C、H元素质量之比为12:1,O氧元素质量分数为8%,则混合物中C、H元素总质量分数为1-8%=92%,故混合物中碳元素质量分数为92%×$\frac{12}{13}$=84.9%,故选D.
点评 本题考查混合物中元素质量分数的计算,关键是根据化学式判断混合物中C、H元素质量之比,难度不大.

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目
20.2001年初,利用制造原子弹的核废料238U(原子序数为92)制成的贫铀弹在欧洲闹得沸沸扬扬.下列有关238U的说法,不正确的是( )
| A. | 238U核外有92个电子 | B. | 238U的原子质量约为12C的238倍 | ||
| C. | 238U原子核内有146个中子 | D. | 238U是U元素的一种核素 |
17.高温下,某反应达到平衡,平衡常数K=$\frac{c(CO)•c({H}_{2}O)}{c(C{O}_{2})•c({H}_{2})}$.恒容时,温度升高,H2浓度减小.下列说法不正确的是( )
| A. | 该反应是焓变为正值 | |
| B. | 恒温恒容下,充入更多的CO2,能提高H2的转化率 | |
| C. | 升高温度,正、逆反应速率均增大 | |
| D. | 该反应化学方程式为:CO+H2O$?_{△}^{催化剂}$ CO2+H2 |
4.短周期主族元素X、Y、Z、W的原子序数依次增大.X原子的最外层电子数是其内层电子数的2倍,Y是地壳中含量最高的元素,Z2+与Y2-具有相同的电子层结构,W与X同主族.下列说法正确的是( )
| A. | W、Z、Y、X的原子半径依次减小 | |
| B. | Y分别与Z、W形成的化合物中化学键类型相同 | |
| C. | X的最高价氧化物对应的水化物的酸性比W的弱 | |
| D. | Y的气态简单氢化物的热稳定性比W的强 |
14.下些列有关电池的说法错误的是( )
| A. | 手机上用的锂离子电池属于二次电池 | |
| B. | 铅酸蓄电池中,铅电极是负极 | |
| C. | 甲醇醇燃料电池可把化学能转化为电能 | |
| D. | 铜锌原电池工作时,Zn2+沿外电路从正极流向负极 |
1.可逆反应 mA(g)+nB(g)?pC(g),在不同温度T、压强p下,生成物C的物质的量分数x(C)的变化情况,如图所示.下列对该反应的判断正确的是( )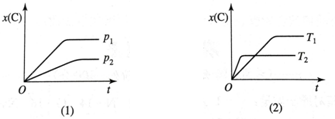

| A. | 吸热反应,m+n<p | B. | 吸热反应,m+n>p | C. | 放热反应,m+n<p | D. | 放热反应,m+n>p |
18.下列说法正确的是( )
| A. | 增大压强,活化分子数增多,化学反应速率一定增大 | |
| B. | 升高温度,活化分子百分数不一定增大,化学反应速率一定增大 | |
| C. | 加入反应物,使活化分子百分数增加,化学反应速率增大 | |
| D. | 使用催化剂,降低了反应的活化能,增大了活化分子百分数,化学反应速率一定增大 |
