题目内容
【题目】已建立化学平衡的某可逆反应X(g)+2Y(g)![]() 2Z(g),当条件改变使化学平衡向正反应方向移动时,下列叙述正确的是
2Z(g),当条件改变使化学平衡向正反应方向移动时,下列叙述正确的是
①生成物的质量分数一定增加,②生成物总量一定增加, ③反应物的转化率一定增大,
④反应物的浓度一定降低,⑤正反应速率一定大于逆反应速率,⑥一定使用催化剂
A.①②③ B.③④⑤ C.②⑤ D.④⑥
【答案】C
【解析】
试题①总质量不变,平衡向正反应移动,生成物的质量分数一定增大,若生成物质量增大小于混合物总质量增大,生成物的质量分数可能降低,故①错误;②平衡向正反应移动,生成物的物质的量一定增加,故②正确;③降低生成物的浓度,平衡向正反应方向移动,反应物的转化率一定增大,但增大某一反应的浓度,平衡向正反应移动,其它反应物的转化率增大,自身转化率降低,故③错误;④如增大反应物的浓度,平衡向正方向移动,达到平衡时,反应物的浓度比改变条件前大,故④错误;⑤平衡向正反应移动,正反应速率一定大于逆反应速率,故⑤正确;⑥加入催化剂,正逆反应速率同等程度增大,平衡不移动,故⑥错误,因此答案选C。

【题目】取0.55mol/L的NaOH溶液50mL与0.25mol/L的硫酸50mL置于下图所示的装置中进行中和热的测定实验。回答下列问题:

(1)从图中实验装置看,其中尚缺少的一种玻璃用品是______________,除此之外,装置中的一个明显错误是_____________________________。
(2)为保证该实验成功该同学采取了许多措施,如图的碎泡沫塑料的作用在于____________________________________。
(3)实验数据如下表:
①请填写下表中的空白:
温度 实验序号 | 起始温度t1(℃) | 终止温度t2(℃) | 温度差平均值 (t2-t1)(℃) | ||
H2SO4 | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 29.5 | ___________ |
2 | 27.0 | 27.4 | 27.2 | 32.3 | |
3 | 25.9 | 25.9 | 25.9 | 29.2 | |
4 | 26.4 | 26.2 | 26.3 | 29.8 | |
②近似认为实验所用溶液的密度都是1 g/cm3,中和后溶液的比热容c=4.18 J/(g·℃)。根据实验结果写出NaOH溶液与HCl溶液反应的热化学方程式(计算结果保留一位小数):_______________。
③上述实验数值结果与57.3 kJ/mol有偏差,产生偏差的原因可能是(填字母)________。
a.实验装置保温、隔热效果差
b.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
(4)如果用含0.5mol Ba(OH)2的稀溶液与足量稀硫酸溶液反应,反应放出的热____57.3 kJ(填“大于”、“小于”或“等于”)。
【题目】二氧化氯(ClO2)常用于处理含硫废水。某学习小组在实验室中探究ClO2与Na2S的反应。
已知:① ClO2是极易溶于水的黄绿色气体,有毒,沸点为11℃。
② SO2 + NaClO3 + H2SO4→ ClO2 + NaHSO4(未配平)
③ ClO2 + NaOH→NaCl + NaClO3 + H2O(未配平)
请回答下列问题:
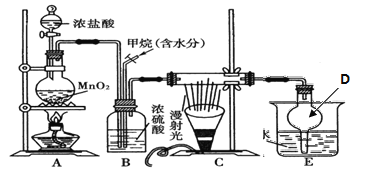
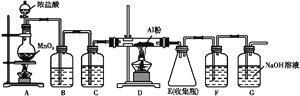
(1)设计如下装置制备ClO2

①装置A中反应的化学方程式为__________________________________。
②装置B中反应的氧化剂与还原剂的物质的量之比为___________。
③欲收集一定量的ClO2,选择上图中的装置,其连接顺序为a→g→h→_________________→d。
(2)探究ClO2与Na2S的反应
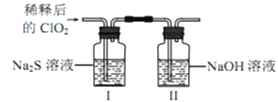
将上述收集到的ClO2用N2稀释以增强其稳定性,并将适量的稀释后的ClO2通入如图所示装置中充分反应,得到无色澄清溶液。一段时间后,通过下列实验探究Ⅰ中反应的产物
操作步骤 | 实验现象 | 结论 |
取少量Ⅰ中溶液放入试管甲中,滴加品红溶液和盐酸。 | 品红溶液始终不褪色 | ①无_______生成。 |
另取少量Ⅰ中溶液放入试管乙中,加入Ba(OH)2溶液和盐酸,振荡。 | ②___________ | 有SO42-生成 |
③继续在试管乙中加入Ba(OH)2溶液至过量,静置,取上层清液放入试管丙中,______________。 | 有白色沉淀生成 | 有Cl-生成 |
④ClO2与Na2S反应的离子方程式为_________________________________________。用于处理含硫废水时,ClO2相对于Cl2的优点是_____________________________________________(任写一条)。