题目内容
【题目】取0.55mol/L的NaOH溶液50mL与0.25mol/L的硫酸50mL置于下图所示的装置中进行中和热的测定实验。回答下列问题:

(1)从图中实验装置看,其中尚缺少的一种玻璃用品是______________,除此之外,装置中的一个明显错误是_____________________________。
(2)为保证该实验成功该同学采取了许多措施,如图的碎泡沫塑料的作用在于____________________________________。
(3)实验数据如下表:
①请填写下表中的空白:
温度 实验序号 | 起始温度t1(℃) | 终止温度t2(℃) | 温度差平均值 (t2-t1)(℃) | ||
H2SO4 | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 29.5 | ___________ |
2 | 27.0 | 27.4 | 27.2 | 32.3 | |
3 | 25.9 | 25.9 | 25.9 | 29.2 | |
4 | 26.4 | 26.2 | 26.3 | 29.8 | |
②近似认为实验所用溶液的密度都是1 g/cm3,中和后溶液的比热容c=4.18 J/(g·℃)。根据实验结果写出NaOH溶液与HCl溶液反应的热化学方程式(计算结果保留一位小数):_______________。
③上述实验数值结果与57.3 kJ/mol有偏差,产生偏差的原因可能是(填字母)________。
a.实验装置保温、隔热效果差
b.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
(4)如果用含0.5mol Ba(OH)2的稀溶液与足量稀硫酸溶液反应,反应放出的热____57.3 kJ(填“大于”、“小于”或“等于”)。
【答案】环形玻璃搅拌棒烧杯口未用硬纸板(或泡沫塑料板)盖住隔热,减少热量的损失3.4NaOH(aq)+1/2H2SO4(aq) =1/2Na2SO4(aq)+H2O(l) ΔH=-56.8 kJ/molabc大于
【解析】
(1)由量热计的构造可知该装置的缺少仪器是环形玻璃搅拌棒;中和热测定实验成败的关键是保温工作,装置中的一个明显错误是烧杯口未用硬纸板(或泡沫塑料板)盖住;
(2)实验中的碎纸条可以起到隔热,减少热量的损失的作用;
(3)①根据标准数据可知,四次温度差分别是(℃)3.4、5.1、3.3、3.5,所以第二次的实验误差太大,舍去。因此温度差的平均值是![]() =3.4℃;
=3.4℃;
②反应中生成水的物质的量是0.0275mol,而反应中放出的热量是(60+50)g×4.18 J/(g·℃)×3.4℃=156.332J,因此中和热△H=-![]() =-56.8kJ/mol;
=-56.8kJ/mol;
③实验数值结果与57.3 kJ/mol相比偏小,这说明反应中有热量的损失,a和c正确。用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度,会使硫酸的起始温度偏高,所以温度差减小,测定结果偏低,所以答案选abc;
(4)中和热是强酸强碱稀溶液中和反应生成1mol水放出的热量,生成硫酸钡沉淀放出热量;表示Ba(OH)2的稀溶液与足量稀硫酸反应放出的热量大于57.3 kJ。

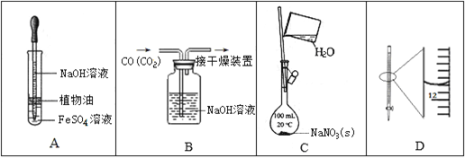
【题目】某学习小组依据反应:SO2(g)+Cl2(g)![]() SO2Cl2(g)△H<0,设计制备磺酰氯SO2Cl2的装置如图:
SO2Cl2(g)△H<0,设计制备磺酰氯SO2Cl2的装置如图:

有关信息如表所示:
SO2Cl2 | Cl2 | SO2 | |
熔点/℃ | -54.1 | -101 | -72.4 |
沸点/℃ | 69.1 | -34.6 | -10 |
性质 | 遇水发生剧烈水解 | / | / |
(1)若用浓盐酸与二氧化锰为原料制取Cl2,反应的化学方程式为 ______。
(2)B仪器的作用是 ______。
(3)为了便于混合物的分离且提高反应物的转化率,A装置的反应条件最好选择 ______。
a.冰水浴 b.常温 c.加热至69.1℃
(4)如果通入的Cl2或SO2含有水蒸气,氯气和二氧化硫可能发生反应的化学方程式为 ______ .
(5)实验时先通入干燥的Cl2将A装置中的空气赶走,再缓慢通入干燥的SO2,即发生反应.充分反应后,继续通入Cl2使装置中的SO2进入烧杯中被吸收。分离产物后,向获得的SO2Cl2中加水,出现白雾,振荡、静置得到无色溶液W。
①经分析SO2Cl2与H2O反应属于非氧化还原反应,写出该反应的化学方程式_________________。
②无色溶液W中的阴离子除含少量OH-外,还含有其它两种阴离子,检验溶液W中这两种阴离子方法是______。
③反应完成后,在W溶液、烧杯中分别滴加过量的BaCl2溶液,均出现白色沉淀,此沉淀不溶于稀盐酸,经过滤、洗涤、干燥,称量得到的固体质量分别为Xg、Yg,计算SO2+Cl2![]() SO2Cl2反应中,SO2的转化率为_____(用含X、Y的代数式表示)。
SO2Cl2反应中,SO2的转化率为_____(用含X、Y的代数式表示)。
【题目】现有一瓶甲和乙的混合物,已知甲和乙的某些性质如下表所示:
物质 | 熔点/ ℃ | 沸点/ ℃ | 密度/ g·cm3 | 水中的溶解性 |
甲 | -98 | 57.5 | 0.93 | 可溶 |
乙 | -84 | 77 | 0.90 | 可溶 |
据此,将甲和乙互相分离的方法是
A. 蒸馏法 B. 升华法 C. 萃取法 D. 过滤法
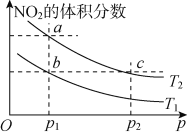
【题目】一定温度下,在三个容积相同的恒容密闭容器中按不同的方式投入反应物,发生反应 N2(g)+3H2(g)![]() 2NH3(g) △H=-92.4kJ/mol,测得反应的相关数据如下表:
2NH3(g) △H=-92.4kJ/mol,测得反应的相关数据如下表:
容器甲 | 容器乙 | 容器丙 | |
反应温度/℃ | 400 | 400 | 500 |
反应物投入量 | 1molN2,3molH2 | 4molNH3 | 1molN2,3molH2 |
平衡时v(正)(H2)/mol/(Ls) | v1 | v2 | v3 |
平衡时c(NH3)/(mol/L) | c1 | c2 | c3 |
平衡时总压强P/Pa | P1 | P2 | P3 |
物质的平衡转化率a | a1(N2) | a2(NH3) | a3(N2) |
平衡常数K | K1 | K2 | K3 |
下列关系正确的是
A. v1<v2,c1<2c2 B. c2>2c3,a2(NH3)+a3(N2)<1
C. K1>K3, P2>2P3 D. v1<v3,a1(N2)<a3(N2)