题目内容
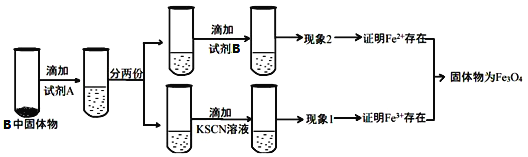
【题目】已知A为淡黄色固体,T为生活中使用最广泛的金属单质,D是具有磁性的黑色晶体,C是无色无味的气体,H是白色沉淀。
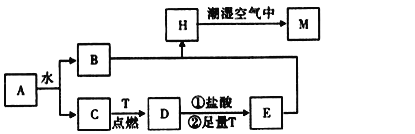
(1)物质A的化学式为 ________。
(2)H在潮湿空气中变成M的实验现象是__________________________________________,化学方程式为___________________________________________。
(3)A和水反应生成B和C的离子方程式为___________________________________,列出A的一种重要用途_________。
(4)反应①的离子方程式为_______________________________________。
【答案】Na2O2 白色沉淀迅速变为灰绿色,最终变为红褐色 4Fe(OH)2 + 2H2O + O2 = 4Fe(OH)3 2Na2O2 + 2H2O = 4Na+ + 4OH- + O2↑ 供氧剂(或漂白剂) Fe3O4+8H+ = Fe2++2Fe3+ + 4H2O
【解析】
根据转化关系和反应条件,A为淡黄色固体且能与水反应,所以A为Na2O2,T为生活中使用最广泛常的金属单质,则T为Fe,D是具有磁性的黑色晶体,则D为Fe3O4,C是无色无味的气体,H是白色沉淀,过氧化钠与水反应生成B和C,铁与C反应生成Fe3O4,所以C为O2,B为NaOH,D与盐酸反应再与铁反应生成E为FeCl2,B与E反应生成H为Fe(OH)2,H与潮湿的空气反应生成M为Fe(OH)3,据此答题。
根据转化关系和反应条件,A为淡黄色固体且能与水反应,所以A为Na2O2,T为生活中使用最广泛常的金属单质,则T为Fe,D是具有磁性的黑色晶体,则D为Fe3O4,C是无色无味的气体,H是白色沉淀,过氧化钠与水反应生成B和C,铁与C反应生成Fe3O4,所以C为O2,B为NaOH,D与盐酸反应再与铁反应生成E为FeCl2,B与E反应生成H为Fe(OH)2,H与潮湿的空气反应生成M为Fe(OH)3,
(1)根据上面的分析可以知道,A为Na2O2,
因此,本题正确答案是:Na2O2;
(2) Fe(OH)2在潮湿空气中变成Fe(OH)3的现象是白色沉淀迅速变为灰绿色,最终变为红褐色,化学方程式为4Fe(OH)2 + 2H2O + O2 = 4Fe(OH)3,
因此,本题正确答案是:白色沉淀迅速变为灰绿色,最终变为红褐色;4Fe(OH)2 + 2H2O + O2 = 4Fe(OH)3;
(3) Na2O2和水反应生成NaOH和O2的离子方程式为2Na2O2 + 2H2O = 4Na+ + 4OH- + O2↑;Na2O2具有强氧化性,可用作供氧剂(或漂白剂),
因此,本题正确答案是:2Na2O2 + 2H2O = 4Na+ + 4OH- + O2↑;供氧剂(或漂白剂);
4)反应①为四氧化三铁和盐酸反应生成氯化铁、氯化亚铁和水,离子方程式为Fe3O4+8H+ = Fe2++2Fe3+ + 4H2O,
因此,本题正确答案是:Fe3O4+8H+ = Fe2++2Fe3+ + 4H2O。

 阅读快车系列答案
阅读快车系列答案