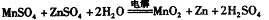题目内容
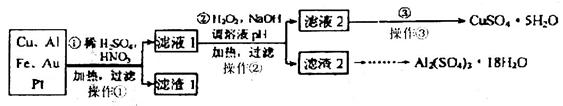
从回收的含铜电缆废料中提取铜时,假若设计如下两种方案,回答有关问题。
方案甲:
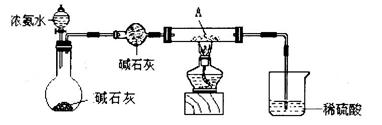
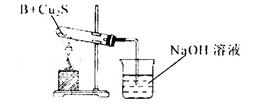
方案乙:
(1)两个方案中,符合当前生产中绿色化学理念的是方案 ,理由是 方案第一步“灼烧”会产生污染空气的气体、粉尘、烟雾。
(2)方案乙中铜溶解生成蓝色溶液时发生反应的离子方程式为________________ _ ______。
(3)为了提高原料的利用率,最后一步所得浅绿色滤液通过蒸发浓缩、冷却结晶、过滤、洗涤、自然干燥可得到一种结晶水合物的晶体。获得晶体后对其进行检测:
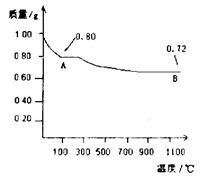
①先取a g的晶体进行脱水实验,获得无水固体为(a—1.26)g
②将无水固体溶于足量的水配成溶液后滴加1.00mol/L的氯化钡溶液,当滴加10.00mL溶液时,沉淀恰好完全。通过计算测知该晶体的化学式是 。
(4)氯化亚铜(CuCl)是重要的化工原料。国家标准规定合格的CuCl产品的主要质量指标为CuCl的质量分数大于96.5% 。工业上用硫酸铜等原料常通过下列反应制备CuCl :
2CuSO4+ Na2SO3 + 2 NaCl + Na2CO3=2 CuCl ↓+ 3 Na2SO4 + CO2↑
测定CuCl质量分数时先准确称取所制备的0.2500g CuCl样品置于一定量的0.5mol·L-1 FeCl3溶液中,待样品完全溶解后,加水20mL,用0.1000mol·L-1 Ce(SO4)2溶液滴定到终点,消耗24.60mL Ce(SO4)2溶液。有关反应的离子方程式为:Fe 3++CuCl=Fe 2++Cu2++Cl- ,Ce4+ + Fe 2+=Fe 3+ + Ce3+
计算上述样品中CuCl的质量分数为 。
(10分)(1)乙 ;甲 (2)2Cu + O2 +4H+ 2Cu2+ + 2H2O (3)FeSO4·7H2O (4)97.9%
2Cu2+ + 2H2O (3)FeSO4·7H2O (4)97.9%
解析试题分析:(1)方案甲中电缆废料在空气中燃烧时能产生污有毒的气体、粉尘、烟雾而污染空气;而方案乙中不燃烧,所以不能产生有毒气体,因此方案乙符合绿色化学理念。
(2)在加热的条件下铜和氧气反应生成氧化铜,氧化铜溶解在稀硫酸中生成硫酸铜,反应的离子方程式为2Cu + O2 +4H+ 2Cu2+ + 2H2O。
2Cu2+ + 2H2O。
(3)取a g的晶体进行脱水实验,获得无水固体为(a—1.26)g,这说明反应中生成的水的质量是1.26g,物质的量是1.26g÷18g/mol=0.07mol;消耗氯化钡的物质的量是0.01mol,白色沉淀是硫酸钡,则根据原子守恒可知,晶体中SO42-的物质的量是0.01mol,所以晶体中硫酸亚铁和结晶水的个数之比是1:7,因此晶体的化学式为FeSO4·7H2O。
(4)根据离子方程式Fe 3++CuCl=Fe 2++Cu2++Cl- ,Ce4+ + Fe 2+=Fe 3+ + Ce3+可知,
CuCl~Fe 2+~Ce4+
1mol 1mol
n 0.0246L×0.1000mol/L
解得n=0.00246mol
所以CuCl的质量=0.00246mol×99.5g/mol=0.24477g
因此上述样品中CuCl的质量分数为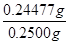 ×100%=97.9%。
×100%=97.9%。
考点:考查绿色化学、晶体化学式确定、物质制备以及物质含量测定的有关计算

 备战中考寒假系列答案
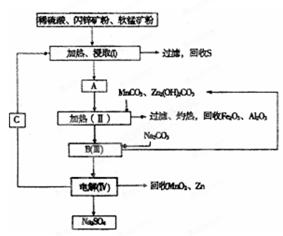
备战中考寒假系列答案从废钒催化剂(主要成分V2O5、VOSO4、K2SO4、SiO2等)中回收V2O5的一种生产工艺流程示意图如下,请回答下列问题:
(1)步骤①中废渣的主要成分是 ,③中X试剂为 。
(2)实验室中进行萃取分液操作时,注入萃取剂,充分振荡,将分液漏斗于铁圈上静置,当液体分层后,接下来的操作是 。
(3)②、③的变化过程可简化为(下式R表示VO2+,HA表示有机萃取剂)。
R2(SO4)n (水层)+ 2nHA(有机层) 2RAn(有机层) + nH2SO4 (水层)为提高②中萃取百分率,应采取的措施是 。
2RAn(有机层) + nH2SO4 (水层)为提高②中萃取百分率,应采取的措施是 。
(4)请完成④中的反应离子方程式:
□ClO3- + □VO2+ +□H+ =□VO3+ + □ +□
(5)25℃时,取样进行试验分析,得到钒沉淀率和溶液pH之间关系如下表:
| pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
| 钒沉淀率% | 88.1 | 94.8 | 96.5 | 98.0 | 98.8 | 98.8 | 96.4 | 93.1 | 89.3 |
结合上表,在实际生产中,⑤中加入氨水,调节溶液的最佳pH值为 。
(6)该工艺流程中,可以循环利用的物质有 。

 2MgO+2SO2↑+CO2↑
2MgO+2SO2↑+CO2↑